��Ŀ����
ij100mL��CuCl2��Һ�У���֪��Һ�е�Cl-��Ũ��Ϊ0.2mol?L-1���ֽ�һ����������Ͷ�뵽����Һ�У�����Ӧ����Һ������䣬�ش��������⣺
��1��ԭ��Һ��Cu2+��Ũ��Ϊ______��
��2����Ӧ����Cl-��Ũ��Ϊ______mol?L-1��
��3����Ӧ����������______����Ӧ������Һ��Fe2+��Ũ��Ϊ0.05mol?L-1����Ӧ����ͭ���ʵ�����Ϊ______g��ת�Ƶ���______����
��4��ʣ���Cu2+�����ʵ���Ũ��Ϊ______��
�⣺��1���ɻ�ѧʽCuCl2��֪��CuCl2��Һ��c��Cu2+��= c��Cl-��=
c��Cl-��= ��0.2mol/L=0.1mol/L���ʴ�Ϊ��0.1mol/L��
��0.2mol/L=0.1mol/L���ʴ�Ϊ��0.1mol/L��
��2������һ���������ۣ�������Ӧ��Fe+Cu2+=Fe2++Cu��Cl-���μӷ�Ӧ��������䣬Cl-Ũ�Ȳ���Ϊ0.2mol/L��
�ʴ�Ϊ��0.2��
��3��������ӦFe+CuCl2=FeCl2+Cu����Ӧ��CuCl2��Cu��CuԪ�ػ��ϼ���+2�۽���Ϊ0�ۣ�CuCl2����������
Fe+Cu2+=Fe2++Cu
0.05mol?L-1��0.1L 0.005mol
��Ӧ����ͭ���ʵ�����Ϊ0.005mol��64g/mol=0.32g��
n��Fe2+��=0.1L��0.05mol/L=0.005mol����Ӧ��Fe��Fe2+�����ϼ���0������Ϊ+2�ۣ�ת�Ƶ������ʵ���Ϊ��0.005mol��2=0.01mol��ת�Ƶ�����ĿΪ��0.01mol��NAmol-1=0.01NA
�ʴ�Ϊ��CuCl2��0.32��0.01NA��
��4��Fe+Cu2+=Fe2++Cu
0.005mol 0.1L��0.05mol/L
ʣ���Cu2+�����ʵ���Ϊ��0.1mol/L��0.1L-0.005mol=0.005mol�������ʵ���Ũ��Ϊ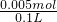 =0.05mol/L��
=0.05mol/L��
�ʴ�Ϊ��0.05mol/L��
��������1���ɻ�ѧʽCuCl2��֪��CuCl2��Һ��c��Cu2+��= c��Cl-����
c��Cl-����
��2������һ���������ۣ�������ӦFe+Cu2+=Fe2++Cu��Cl-���μӷ�Ӧ��������䣬Cl-Ũ�Ȳ��䣻
��3������Ԫ�ػ��ϼ۽��͵ķ�Ӧ�������������������ӷ���ʽFe+Cu2+=Fe2++Cu�����㣻��Ӧ��Fe��Fe2+�����ϼ���0������Ϊ+2�ۣ�ת�Ƶ������ʵ���ΪFe2+�����ʵ���2��������N=nNA����ת�Ƶ�����Ŀ��
��4���������ӷ���ʽFe+Cu2+=Fe2++Cu�������ʣ��Cu2+�����ʵ�����Ȼ�������Ũ�ȣ�
���������⿼�����ӷ���ʽ����д��������ԭ��Ӧ�����������йؼ��㡢���û�ѧ�������йؼ���ȣ��ѶȲ���ע�����֪ʶ�����գ�
 c��Cl-��=
c��Cl-��= ��0.2mol/L=0.1mol/L���ʴ�Ϊ��0.1mol/L��
��0.2mol/L=0.1mol/L���ʴ�Ϊ��0.1mol/L����2������һ���������ۣ�������Ӧ��Fe+Cu2+=Fe2++Cu��Cl-���μӷ�Ӧ��������䣬Cl-Ũ�Ȳ���Ϊ0.2mol/L��
�ʴ�Ϊ��0.2��
��3��������ӦFe+CuCl2=FeCl2+Cu����Ӧ��CuCl2��Cu��CuԪ�ػ��ϼ���+2�۽���Ϊ0�ۣ�CuCl2����������
Fe+Cu2+=Fe2++Cu
0.05mol?L-1��0.1L 0.005mol
��Ӧ����ͭ���ʵ�����Ϊ0.005mol��64g/mol=0.32g��
n��Fe2+��=0.1L��0.05mol/L=0.005mol����Ӧ��Fe��Fe2+�����ϼ���0������Ϊ+2�ۣ�ת�Ƶ������ʵ���Ϊ��0.005mol��2=0.01mol��ת�Ƶ�����ĿΪ��0.01mol��NAmol-1=0.01NA
�ʴ�Ϊ��CuCl2��0.32��0.01NA��
��4��Fe+Cu2+=Fe2++Cu
0.005mol 0.1L��0.05mol/L
ʣ���Cu2+�����ʵ���Ϊ��0.1mol/L��0.1L-0.005mol=0.005mol�������ʵ���Ũ��Ϊ
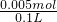 =0.05mol/L��
=0.05mol/L���ʴ�Ϊ��0.05mol/L��
��������1���ɻ�ѧʽCuCl2��֪��CuCl2��Һ��c��Cu2+��=
 c��Cl-����
c��Cl-������2������һ���������ۣ�������ӦFe+Cu2+=Fe2++Cu��Cl-���μӷ�Ӧ��������䣬Cl-Ũ�Ȳ��䣻
��3������Ԫ�ػ��ϼ۽��͵ķ�Ӧ�������������������ӷ���ʽFe+Cu2+=Fe2++Cu�����㣻��Ӧ��Fe��Fe2+�����ϼ���0������Ϊ+2�ۣ�ת�Ƶ������ʵ���ΪFe2+�����ʵ���2��������N=nNA����ת�Ƶ�����Ŀ��
��4���������ӷ���ʽFe+Cu2+=Fe2++Cu�������ʣ��Cu2+�����ʵ�����Ȼ�������Ũ�ȣ�
���������⿼�����ӷ���ʽ����д��������ԭ��Ӧ�����������йؼ��㡢���û�ѧ�������йؼ���ȣ��ѶȲ���ע�����֪ʶ�����գ�

��ϰ��ϵ�д�
 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
�����Ŀ