题目内容
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图,下列表述中正确的是( )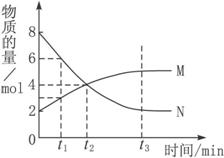
A.反应的化学方程式为![]() N B.t2时,正、逆反应速率相等,达到平衡
N B.t2时,正、逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率 D.t1时,N的浓度是M浓度的2倍
解析:从反应开始到t1时刻,N消耗2 mol,同时生成M 1 mol,根据“化学计量数之比等于物质的量的变化量之比”可得化学方程式为2N![]() M。在t2时仅为“物质的量”或“物质的量浓度”相等,而非速率相等。t3时各物质的量不再变化,已达反应限度,正逆反应速率相等。N原有8 mol,M原有2 mol,在t1时N为6 mol,M为3 mol,N的浓度是M浓度的2倍。
M。在t2时仅为“物质的量”或“物质的量浓度”相等,而非速率相等。t3时各物质的量不再变化,已达反应限度,正逆反应速率相等。N原有8 mol,M原有2 mol,在t1时N为6 mol,M为3 mol,N的浓度是M浓度的2倍。
答案:D

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
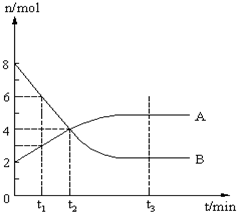 在一定温度下,容器内某反应物中A、B的物质的量随反应时间变化的曲线如图.下列表述正确的是( )
在一定温度下,容器内某反应物中A、B的物质的量随反应时间变化的曲线如图.下列表述正确的是( )| A、t1时,C(A)=2 C(B) | B、t2时,v(正)=v(逆),达到平衡 | C、t3时,v(正)=v(逆) | D、该反应的化学方程式为:2A=B |
 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列叙述正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列叙述正确的是( )| A、反应的方程式为M?2N | B、t1时,N的浓度是M浓度的0.5倍 | C、t2时,正逆反应速率相等,达到平衡 | D、t3时,正反应速率大于逆反应速率 |
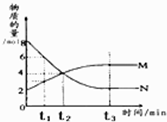 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A、反应的化学方程式为:N?2M | B、t2时,反应不再发生 | C、t2时,正反应速率等于逆反应速率 | D、t3后,反应到达最大限度 |
 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )