题目内容
 在一定温度下,容器内某一反应中M、N的物质的量随反应时间的变化曲线如图,下列表述中不正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间的变化曲线如图,下列表述中不正确的是( )分析:A.根据图象判断出反应物和生成物,根据物质的量的变化判断计量数之间的关系;
B.t3时,各物质的物质的量不变;
C.t2时,为正反应速率大于逆反应速率,反应没有达到平衡;
D.根据某一时刻反应物和生成物的物质的量多少判断浓度的关系.
B.t3时,各物质的物质的量不变;
C.t2时,为正反应速率大于逆反应速率,反应没有达到平衡;
D.根据某一时刻反应物和生成物的物质的量多少判断浓度的关系.
解答:解:A.由图象可知,反应中M的物质的量逐渐增多,N的物质的量逐渐减少,则在反应中N为反应物,M为生成物,图象中,在相等的时间内消耗的N和M的物质的之比为2:1,所以反应方程式应为:2N M,故A错误;
M,故A错误;
B.t3时,各物质的物质的量不变,为平衡状态,正逆反应速率相等,故B正确;
C.t2时,为正反应速率大于逆反应速率,反应没有达到平衡,则N的消耗速率大于N的生成速率,故C正确;
D.t1时,N的物质的量为6mol.M的物质的量为3mol,故N的浓度是M浓度的2倍,故D正确;
故选A.
 M,故A错误;
M,故A错误;B.t3时,各物质的物质的量不变,为平衡状态,正逆反应速率相等,故B正确;
C.t2时,为正反应速率大于逆反应速率,反应没有达到平衡,则N的消耗速率大于N的生成速率,故C正确;
D.t1时,N的物质的量为6mol.M的物质的量为3mol,故N的浓度是M浓度的2倍,故D正确;
故选A.
点评:本题考查化学反应速率与化学平衡知识,注意从反应物和生成物的物质的量的变化角度,判断反应物和生成物以及反应是否达到平衡,题目难度不大.

练习册系列答案
相关题目
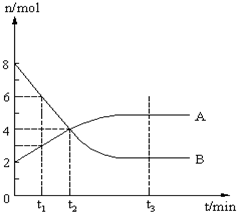 在一定温度下,容器内某反应物中A、B的物质的量随反应时间变化的曲线如图.下列表述正确的是( )
在一定温度下,容器内某反应物中A、B的物质的量随反应时间变化的曲线如图.下列表述正确的是( )| A、t1时,C(A)=2 C(B) | B、t2时,v(正)=v(逆),达到平衡 | C、t3时,v(正)=v(逆) | D、该反应的化学方程式为:2A=B |
 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列叙述正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列叙述正确的是( )| A、反应的方程式为M?2N | B、t1时,N的浓度是M浓度的0.5倍 | C、t2时,正逆反应速率相等,达到平衡 | D、t3时,正反应速率大于逆反应速率 |
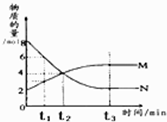 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A、反应的化学方程式为:N?2M | B、t2时,反应不再发生 | C、t2时,正反应速率等于逆反应速率 | D、t3后,反应到达最大限度 |