题目内容
14.下列有关原子知识的叙述正确的是( )| A. | 原子是构成一切物质的微粒 | |
| B. | 原子是化学变化中的最小微粒 | |
| C. | 原子是构成物质的一种微粒 | |
| D. | 原子是保持物质化学性质的最小微粒 |
分析 分子是保持物质化学性质的最小粒子,而原子是化学变化中的最小粒子,分子与原子的本质区别:在化学变化中是否可分.
解答 解:A.分子、原子、离子都是构成物质的基本粒子,故A错误;
B.化学变化中的最小粒子是原子,故B正确;
C.分子、原子、离子都是构成物质的基本粒子,原子是构成物质的一种微粒,故C正确;
D.分子是保持物质化学性质的最小粒子才是保持物质化学性质的最小粒子,故D错误.
故选BC.
点评 本题考查原子构成,难度不是很大,注意分子和原子的区别和联系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.加热mg质量分数相等的Na2CO3和NaHCO3混合物,一段时间后,质量变为ng,当NaHCO3完全分解时,n的值为( )
| A. | $\frac{53m}{168}$ | B. | $\frac{137m}{168}$ | C. | $\frac{53m}{84}$ | D. | $\frac{159m}{168}$ |
5.反应4NH3+5O2?4NO+6H2O在5L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率表达正确的是( )
| A. | v(O2)=0.01 mol•(L•s)-1 | B. | v(NO)=0.008 mol•(L•s)-1 | ||
| C. | v(H2O)=0.003 mol•(L•s)-1 | D. | v(NH3)=0.003 mol•(L•s)-1 |
9.已知:CH4(g)+2O2(g)═CO2(g)+2H2O(1)△H1=-Q1 KJ/mol
2H2(g)+O2(g)═2H2O(g)△H2=-Q2 KJ/mol
2H2(g)+O2(g)═2H2O(1)△H3=-Q3KJ/mol
常温下,取体积比为4:1的甲烷和氢气的混合气体11.2L(已折合成标准状况),经完全燃烧后恢复至常温,则下列说法正确的是( )
2H2(g)+O2(g)═2H2O(g)△H2=-Q2 KJ/mol
2H2(g)+O2(g)═2H2O(1)△H3=-Q3KJ/mol
常温下,取体积比为4:1的甲烷和氢气的混合气体11.2L(已折合成标准状况),经完全燃烧后恢复至常温,则下列说法正确的是( )
| A. | 放出的热量为(0.4Q1+0.1Q3)KJ | B. | 放出的热量为(0.4Q1+0.05Q2)KJ | ||
| C. | 放出的热量为(0.4Q1+0.05Q3)KJ | D. | △H2<△H3 |
3.如图是恒温下某化学反应的反应速率随反应时间变化的示意图.下列叙述与示意图不相符合的是( )
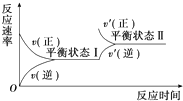

| A. | 反应达平衡时,正反应速率和逆反应速率相等 | |
| B. | 该反应达到平衡状态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡状态Ⅱ | |
| C. | 该反应达到平衡状态Ⅰ后,减小反应物浓度,平衡发生移动,达到平衡状态Ⅱ | |
| D. | 同一种反应物在平衡状态Ⅰ和平衡状态Ⅱ时浓度不相等 |
4.下列保存物质的方法正确的是( )
| A. | 液氯贮存在干燥的钢瓶里 | |
| B. | 少量的锂、钠、钾均保存在煤油中 | |
| C. | 浓溴水保存在带橡皮塞的棕色细口瓶中 | |
| D. | 用排水法收集满一瓶氢气,用玻璃片盖住瓶口,瓶口朝上放置 |
 在高温下,Fe与水蒸气可发生反应.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验“.请回答该实验中的问题.
在高温下,Fe与水蒸气可发生反应.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验“.请回答该实验中的问题.