题目内容
表示0.1mol?L-1 NaHCO3溶液中有关微粒浓度的关系式中不正确的( )
分析:NaHCO3溶液呈碱性,溶液中HCO3-水解程度大于HCO3-电离程度,结合溶液中物料守恒和电荷守恒解答该题.
解答:解:A.溶液呈碱性,所以c (OH-)>c (H+),钠离子不水解,碳酸氢根离子水解,所以c(Na+)>c (HCO3-),盐中阴阳离子浓度大于水电离出氢氧根离子浓度,所以离子浓度大小顺序是c(Na+)>c (HCO3-)>c (OH-)>c (H+),故A正确;
B.根据质子守恒得c(OH-)=2c (H2CO3)+c (CO32-)+c (H+),故B错误;
C.根据电荷守恒得c(Na+)+c (H+)=c (HCO3-)+2 c (CO32-)+c (OH-),故C正确;
D.根据物料守恒得c(Na+)=c (HCO3-)+c (CO32-)+c (H2CO3),故D正确;
故选B.
B.根据质子守恒得c(OH-)=2c (H2CO3)+c (CO32-)+c (H+),故B错误;
C.根据电荷守恒得c(Na+)+c (H+)=c (HCO3-)+2 c (CO32-)+c (OH-),故C正确;
D.根据物料守恒得c(Na+)=c (HCO3-)+c (CO32-)+c (H2CO3),故D正确;
故选B.
点评:本题考查离子浓度的大小比较,题目难度中等,注意把握弱电解质的电离和盐类水解的原理,从守恒的角度比较离子浓度大小是常用的方法.

练习册系列答案
相关题目
室温时,下列各表述与示意图一致的是( )
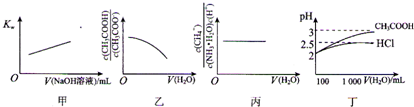

| A、图甲表示在纯水中加入0.01 moL?L-1 NaOH溶液,Kw与NaOH溶液体积变化关系 | ||
B、图乙表示将1 mol?L-1 CH3COONa溶液加水稀释,溶液中
| ||
C、图丙表示0.1mol?L-1 NH3?H2O加水稀释,溶液中
| ||
| D、图丁表示100 mL pH=2的HCl和CH3COOH加水稀释到1000mL时pH变化与水的体积的变化关系 |