题目内容
将含有MnO4-、Fe3+、Fe2+、I-的四种溶液混合,调整溶液的pH值,使pH=1,充分反应后:
(1)若I-离子在溶液中有剩余,则上述四种离子在溶液中还存在的有________,一定不存在的是________
(2)若所得混合液呈紫色,则上述四种离子在溶液中一定存在的有________,一定不存在的离子有________.
解析:
|
(1)Fe2+ MnO-6,Fe3+ (2)MnO-6,Fe3+ Fe2+ I- |

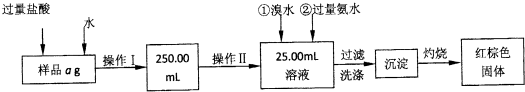
(12分) A、B、C、D、E、F六种化合物。其中A、B、C、D、E均由短周期元素组成,焰色反应均呈黄色,B、C、E均由三种元素组成,B、C的组成元素相同,且C的摩尔质量比B大80g/mol请回答下列问题:
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为 (填序号)。
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(2)下表为B与F实验的部分内容:
| 序号 | 主要实验步骤及实验现象 |
| ① | 在含有B的溶液中,加入稀H2S04,产生浅黄色浑浊和无色有刺激性气味的气体。 |
| ② | 20 ml沸水中滴加F的饱和溶液1~2ml,所得液体呈红褐色 |
| ③ | 将实验②得到的红褐色液体加热蒸发、灼烧,最终得到红棕色固体 |
写出②中反应的化学方程式: 。
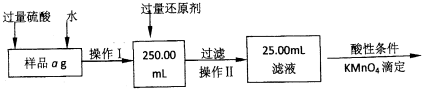
(3)现由6种粒子Mn2+、MnO4一、H十、H2 0、X2Y82一(C中含有的阴离子)、XY42一完成一个离子方程式,已知Mn2+为还原剂,得到1mol MnO4一需氧化剂的物质的量为 。
(4)化合物D和E可以相互转化:
 若有D和E·XH20的混合物13.04g,加热到完全反应后,气体产物通过浓H2S04增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为 ,E·XH20的化学式为 。
若有D和E·XH20的混合物13.04g,加热到完全反应后,气体产物通过浓H2S04增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为 ,E·XH20的化学式为 。 (12分) A、B、C、D、E、F六种化合物。其中A、B、C、D、E均由短周期元素组成,焰色反应均呈黄色,B、C、E均由三种元素组成,B、C的组成元素相同,且C的摩尔质量比B大80g/mol请回答下列问题:
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为 (填序号)。
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(2)下表为B与F实验的部分内容:
|
序号 |
主要实验步骤及实验现象 |
|
① |
在含有B的溶液中,加入稀H2S04,产生浅黄色浑浊和无色有刺激性气味的气体。 |
|
② |
20 ml沸水中滴加F的饱和溶液1~2ml,所得液体呈红褐色 |
|
③ |
将实验②得到的红褐色液体加热蒸发、灼烧,最终得到红棕色固体 |
写出B与稀H2S04反应的离子方程式: ;
写出②中反应的化学方程式: 。
(3)现由6种粒子Mn2+、MnO4一、H十、H2 0、X2Y82一(C中含有的阴离子)、XY42一完成一个离子方程式,已知Mn2+为还原剂,得到1mol MnO4一需氧化剂的物质的量为 。
(4)化合物D和E可以相互转化: 若有D和E·XH20的混合物13.04g,加热到完全反应后,气体产物通过浓H2S04增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为
,E·XH20的化学式为
。
若有D和E·XH20的混合物13.04g,加热到完全反应后,气体产物通过浓H2S04增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为
,E·XH20的化学式为
。