题目内容
【物质结构与性质】
原子序数小于36的X、Y、Z和铜四种元素,X的基态原子有3个不同的能级,有一个能级中的电子数比其它两个能级中的电子数都多1;Y基态原子中的电子占有5个轨道,其中有2个轨道处于半充满状态,Z的原子序数为24。
(1)Z原子基态核外电子排布式为______________________________;
(2)元素X与Y的第一电离能较大的是_________(填元素符号);H2Y2中Y原子轨道的杂化类型为____;
(3)+3价Z的配合物K[Z(C2O4)2(H2O)2]中的配体是_________;与C2O42-互为等电子体的一种分子的化学式为_____________;
(4)Cu和Y形成的化合物的晶胞如图所示,晶胞中与铜离子距离相等且最近的铜离子有_______个.某种有缺陷的铜和Y形成的化合物的晶体由Cu2+、Cu3+、Y2-及空隙组成,可表示为Cu0.98Y,则n(Cu2+)/n(Cu3+)=_______________。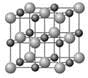
练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
相同温度下,容积相同的3个恒温密闭容器中发生可逆反应:
N2(g)+3H2(g) 2NH3(g) ΔH=-92.6KJ·mol-1
2NH3(g) ΔH=-92.6KJ·mol-1
实验测得起始、平衡时的有关数据如下表:
容器编号 | 起始各物质的物质的量/mol | 达平衡时体系能量的变化 | |||
N2 | H2 | NH3 | Ar | ||
① | 1 | 3 | 0 | 0 | 放出热量:Q1 |
② | 0.9 | 2.7 | 0.2 | 0 | 放出热量:Q2 |
③ | 0.9 | 2.7 | 0.2 | 0.1 | 放出热量:Q3 |
下列比较正确的是
A. 放出热量大小:Q1>Q2=Q3
B. 容器中的压强:③>①=②
C. N2的转化率:①<②<③
D. 平衡时NH3的体积分数:①=②<③


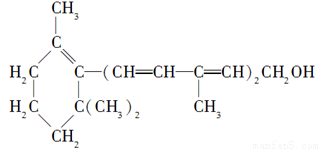
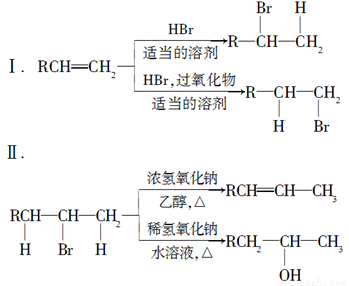

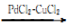 2CH3CHO。下列有关说法正确的是
2CH3CHO。下列有关说法正确的是