题目内容
11.1mg锎(25298Cf)每秒种能释放2.34×109个中子,其在医学上常被用作治疗恶性肿瘤的中子源.下列有关说法错误的是( )| A. | 锎位于元素周期表第七周期 | |
| B. | 1 mg锎(25298Cf)中含有2.34×109个中子 | |
| C. | 25298Cf原子中,质子数和核外电子数均为98 | |
| D. | 25298Cf的中子数与质子数之差为56 |
分析 锎(25298Cf)质子数=核电荷数=原子序数=98,个电子层,原子核外有7位于元素周期表中的第七周期,原子中中子数=质量数-质子数,质子数=核电荷数=核外电子数=原子序数.
解答 解:A.锎(25298Cf)质子数=核电荷数=原子序数=98,个电子层,原子核外有7位于元素周期表中的第七周期,故A正确;
B.质子数为98,质量数为252,中子数=252-98=154,1 mg锎(25298Cf)中含有中子数=154×6.02×1023=9.27×1021个,故B错误;
C.质子数=核电荷数=原子序数,25298Cf原子中,质子数和核外电子数均为98,故C正确;
D.质子数为98,质量数为252,中子数=质量数-质子数,中子数与质子数之差为154-98=56,故D正确;
故选B.
点评 本题考查核素,明确原子中的数量关系即可解答,注意原子构成中不同位置的数字的意义,题目难度不大.

练习册系列答案
相关题目
20.下列化学用语或模型正确的是( )
| A. | 羟基的电子式: | B. | N2的结构式:N≡N | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | CH4分子的球棍模型: |
19.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.5mol羟基中所含电子数为5NA | |
| B. | 1mol苯乙烯( )分子中含有碳碳双键的个数为4NA )分子中含有碳碳双键的个数为4NA | |
| C. | 标准状况下,11.2L的二氯甲烷所含的分子数为0.5NA | |
| D. | 常温下,7.8 gNa2O2中含有的离子总数为0.3NA |
6.某有机物的结构简式为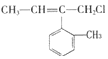 ,则该物质不能发生的反应有( )
,则该物质不能发生的反应有( )
 ,则该物质不能发生的反应有( )
,则该物质不能发生的反应有( )| A. | 加成反应 | B. | 氧化反应 | C. | 取代反应 | D. | 消去反应 |
16.下列关于苯的说法中正确的是( )
| A. | 苯与H2在一定条件下的加成产物环己烷( )中,所有碳原子在同一平面上 )中,所有碳原子在同一平面上 | |
| B. |  可以用于表示苯的分子结构,但是其中并不含有碳碳双键,因此苯的性质跟烯烃不相同 可以用于表示苯的分子结构,但是其中并不含有碳碳双键,因此苯的性质跟烯烃不相同 | |
| C. | 苯的分子式是C6H6,苯分子中的碳原子远没有饱和,因此能与溴水发生加成反应而使之褪色 | |
| D. | 苯环上的碳碳键是一种介于单键和双键之间的独特的键,因此苯可以发生取代反应不能发生加成反应 |
3.设NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 18 gD2O含电子数目为10NA | |
| B. | 1 L 0.1 mol/L NH4NO3溶液中含有氮原子数目为0.2 NA | |
| C. | 0.1 mol CaC2固体含离子数目为0.3 NA | |
| D. | agC2H4和C3H6混合气体含原予数目为aNA/14 |
20.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,6.0g NO和2.24L O2混合,所得气体的分子数目为0.2NA | |
| B. | 常温常压下,0.1mol Na2O和Na2O2组成的混合物中,阴离子的数目为0.1NA | |
| C. | C2H4和C3H6的混合物的质量为mg,所含碳氢键的数目为$\frac{3m}{14}$NA | |
| D. | 1mol甲基( )所含的电子数为7NA )所含的电子数为7NA |
19.下列用电子式表示物质形成过程正确的是:( )
| A. | 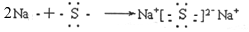 | B. |  | ||
| C. |  | D. |  |
