题目内容
实验探究:
通过实验事实的验证与讨论,认识苯的结构式.提出问题:苯分子结构是碳碳单双键交替的结构吗?
(1)提出假设:从苯的分子式看,C6H6具有不饱和性;从苯的凯库勒结构式看,分子中含有碳碳双键,所以,苯一定能使________褪色;
(2)实验验证:
①苯不能使________褪色;
②经科学测定,苯分子里6个碳原子之间的键________(填“相同”或“不同”);6个碳原子和6个氢原子都在同一________上;
(3)结构:苯的凯库勒结构式中的双键跟烯烃的双键________(填“相同”或“不同”);苯的性质没有表现出不饱和性,结构稳定,说明苯分子________(填“有”或“没有”)一般的碳碳单、双键交替的环状结构.
(4)应用:为了表示苯分子的结构特点,结构简式用________表示,而凯库勒式表示苯分子结构是不确切的.
解析:
|
(共7分)(1)溴水(酸性KMnO4溶液) (2)①溴水(酸性KMnO4溶液) ②相同;平面 (3)不同;没有 (4) |

 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案(10分)兴趣小组通过实验探究溶解铜的方法和本质。
(1)将铜粉分别加入到稍过量的氯化铁溶液和硫酸铁溶液中,铜粉溶解,溶液变成浅绿色,两个反应的共同点是(用离子方程式表示) 。
(2)在热水浴中进行4个实验,部分实验报告如下表所示。
| 序号 | 实验操作 | 实验现象 |
| Ⅰ | 稀硫酸中加入铜片 | 无明显变化 |
| Ⅱ | 硝酸钠溶液中加入铜片] | 无明显变化 |
| Ⅲ |
| 无明显变化 |
| Ⅳ | 稀硫酸中加入硝酸钠溶液 | 无明显变化 |
| 再加入铜片 | 有无色气泡;溶液变蓝 |
①实验操作Ⅲ是 。
②实验I、II、III的目的是 。
③实验Ⅳ中反应的本质是(用离子方程式表示) 。
(3)将铜粉加入到混有硫酸的过氧化氢溶液中,溶液逐渐变成蓝色,该反应的离子方程式是 。
(14分)苯甲酸甲酯是一种重要的工业原料,有机化学中通过酯化反应原理,可以进行苯甲酸甲酯的合成。有关物质的物理性质、实验装置如下所示:
| | 苯甲酸 | 甲醇 | 苯甲酸甲酯 |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |
在大试管中加入15g苯甲酸和一定量的甲醇,边振荡边缓慢加入一定量浓硫酸,按图A连接仪器并实验。
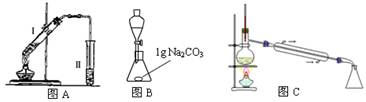
(1)苯甲酸与甲醇反应的化学方程式为_______________ _________。
(2)大试管Ⅰ中除了装有15g苯甲酸和一定量的甲醇和一定量浓硫酸外还需要加入
。
(3)中学实验室中制取乙酸乙酯时为了提高酯的产率可以采取的措施有
__________________ ________ 。
实验二:提纯苯甲酸甲酯
该实验要先利用图B装置把图A中制备的苯甲酸甲酯水洗提纯,再利用图C装置进行蒸馏提纯
(4)用图B装置进行水洗提纯时,B装置中固体Na2CO3作用是 。
(5)用图C装置进行蒸馏提纯时,当温度计显示______时,可用锥形瓶收集苯甲酸甲酯。
实验三:探究浓硫酸在合成苯甲酸甲酯中的作用
(6)比较有、无浓硫酸存在条件下酯化反应进行的快慢,在其他实验条件相同时需要测量的实验数据是 。
(10分)兴趣小组通过实验探究溶解铜的方法和本质。
(1)将铜粉分别加入到稍过量的氯化铁溶液和硫酸铁溶液中,铜粉溶解,溶液变成浅绿色,两个反应的共同点是(用离子方程式表示) 。
(2)在热水浴中进行4个实验,部分实验报告如下表所示。
|
序号 |
实验操作 |
实验现象 |
|
Ⅰ |
稀硫酸中加入铜片 |
无明显变化 |
|
Ⅱ |
硝酸钠溶液中加入铜片] |
无明显变化 |
|
Ⅲ |
|
无明显变化 |
|
Ⅳ |
稀硫酸中加入硝酸钠溶液 |
无明显变化 |
|
再加入铜片 |
有无色气泡;溶液变蓝 |
①实验操作Ⅲ是 。
②实验I、II、III的目的是 。
③实验Ⅳ中反应的本质是(用离子方程式表示) 。
(3)将铜粉加入到混有硫酸的过氧化氢溶液中,溶液逐渐变成蓝色,该反应的离子方程式是 。
如图1所示,某兴趣小组同学将铜片加入稀硝酸,发现开始时气泡产生速率非常慢,一段时间后速率明显加快,烧瓶内溶液呈浅蓝色并不断加深,液面上方的气体颜色也在不断加深。该小组同学拟通过实验探究反应速率变化的原因。

图 1 图 2
(1) 图1中铜与稀硝酸反应的离子方程式为 ;
用离子方程式表示NaOH溶液所起的作用 ;
(2) 小组同学提出了如下假设并设计实验探究:
Ⅰ. 甲同学认为是反应放热导致溶液温度升高所致,完成此实验还需要的仪器是 ;
测定反应过程中溶液不同时间的温度,结果如下表:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 35 | 50 | 60 | 70 | 80 |
| 温度/℃ | 25 | 26 | 26 | 26 | 26 | 26 | 26.5 | 27 | 27 | 27 | 27 |
结合实验目的和表中数据,你得出的结论是 ;
Ⅱ. 乙同学认为生成的Cu2+对反应有催化作用,为验证此假设,取A、B两支试管分别加入等量的铜片和稀硝酸,那么最好是在其中一支试管中加入少量的 (填序号),
A. 硝酸铜晶体 B. 硝酸铜溶液 C. 硫酸铜晶体 D. 硫酸铜溶液
然后对比两支试管的反应,发现现象基本相同。因此得出结论:Cu2+并不是反应的催化剂。
Ⅲ. 丙同学根据现象推测反应过程中还有少量 生成,进而认为该物质对反应有催化作用,如图2所示,实验中丙同学从a处通入该物质后,发现左管中产生气泡速率明显快于右管。小组同学得出最后结论:这种物质对铜和稀硝酸的反应有催化作用。
(3)实验结束后,发现试管中溶液呈绿色,而不显蓝色。部分同学认为是该溶液中硝酸铜的质量分数较高所致,另一部分同学认为是该溶液中溶解了通入的物质。请你设计一个实验方案来证明哪种假设正确。(写出实验操作、实验现象和结论)
。