题目内容
10.(1)现有以下物质①NaCl溶液 ②干冰(固态的二氧化碳) ③冰醋酸(纯净的醋酸) ④铜 ⑤BaSO4固体 ⑥蔗糖 ⑦酒精 ⑧熔融的KNO3 ⑨氢氧化钠固体
其中能导电的是:①④⑧ 属于电解质的是:③⑤⑧⑨ 属于非电解质的是:②⑥⑦
(2)将下列离子Na+、K+、Cu2+、H+、NO3-、Cl-、CO32-、OH-按可能大量共存于同一溶液的情况,把他们分成A、B两组,而且每组中均含两种阳离子和两种阴离子.
A组:Cu2+、H+、Cl-、NO3- B组:Na+、K+、OH-、CO32-(A、B可对换).
分析 (1)能导电的物质必须含有自由电子或自由离子;电解质:在水溶液里或熔融状态下能导电的化合物;非电解质:在水溶液里或熔融状态下都不能导电的化合物,据此进行判断;
(2)根据所有的钠和钾、硝酸根离子形成的化合物都溶于水,碳酸根离子能够和铜离子结合成沉淀,和氢离子结合成水和二氧化碳,氢氧根离子和铜离子结合成氢氧根离子,和氢离子结合成水进行分析.
解答 解:(1)①NaCl溶液是电解质氯化钠的水溶液,它能够导电;⑧熔融的硝酸钾中存在自由的钾离子和硝酸根离子,能够导电;④铜属于金属,能够导电,所以能够导电的有①④⑧;
电解质在水溶液或熔化状态下能够导电的化合物,③冰醋酸水溶液能够导电,冰醋酸属于电解质;⑤硫酸钡的水溶液不能导电,是因为硫酸钡的溶解度太小,硫酸钡属于电解质;⑧熔融状态的硝酸钾因电离出钾离子和氯酸根离子而导电,因而硝酸钾属于电解质;⑨氢氧化钠固体在水溶液和熔融状态下都能够导电,所以属于电解质的为③⑤⑧⑨;
非电解质是指在水溶液里和熔化状态下都不能导电的化合物,蔗糖、酒精水溶液不导电,属于非电解质;干冰即二氧化碳的水溶液能导电,是因为二氧化碳与水反应生成了电解质碳酸,不是二氧化碳本身的缘故,因此干冰属于非电解质,即属于非电解质的只有②⑥⑦,
故答案为:①④⑧;③⑤⑧⑨;②⑥⑦;
(2)设A组中含有Cu2+,Cu2+与CO32-、OH-分别反应生成沉淀而不能共存,CO32-、OH-则应存在于B组中,CO32-、OH-与H+反应而不能共存,则H+应存在于A组,
又每组中均含两种阳离子和两种阴离子,
所以A组中应还含有NO3-、Cl-,B组中还应含有Na+、K+,
所以A组中含有Cu2+、H+、Cl-、NO3-,B组中含有Na+、K+、OH-、CO32- ( A、B可对换),
故答案为:Cu2+、H+、Cl-、NO3-;Na+、K+、OH-、CO32- ( A、B可对换).
点评 本题考查了离子共存的应用、电解质与非电解质及溶液导电性判断,题目难度中等,注意掌握离子反应发生条件,明确电解质与非电解质的区别,试题侧重基础知识的考查,培养了学生的灵活应用能力.

| A. | 混合气体的颜色不再改变 | |
| B. | 混合气体的密度不再改变 | |
| C. | 混合气体的压强不再改变 | |
| D. | 混合气体的平均相对分子质量不再改变 |
| A. | KMnO4→K2MnO4 | B. | HCl→Cl2 | C. | Fe3+→Fe2+ | D. | Na2O→NaOH |
| A. | 在中毒过程中血红蛋白被氧化 | B. | 解毒时血红蛋白被还原 | ||
| C. | 维生素C应具有还原性 | D. | 中毒时亚硝酸盐发生氧化反应 |
| A. | Cu2+、Cl-、K+、SO42- | B. | CO32-、Na+、K+、SO42- | ||
| C. | Mg2+、Cl-、K+、NO3- | D. | Ag+、NO3-、K+、Cl- |
| A. | 钠与水反应:Na+2H2O═Na++OH-+H2↑ | |
| B. | 铁与硫酸铜溶液反应:Fe+Cu2+═Fe2++Cu | |
| C. | 碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓ |
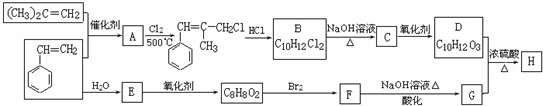
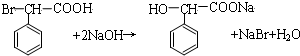 .
.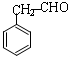 .
.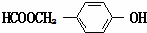 (写结构简式).
(写结构简式).