题目内容
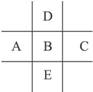
下图为周期表的一部分,已知A、B、C、D、E共有85个电子,E原子核外有4个电子层,则B元素是…………( )
A. P
B. Mg
C. Cl
D. Si
答案:A
解析:
解析:
| 解析:由于E是第四周期元素,且A、B、E处于同一主族。根据这五种元素的排列情况,A、B、E只能处于ⅡA到ⅧA族。若它们处于ⅡA族,设B的原子序数为x,则A、E、C、D的原子序数依次为x—8,x+8,x—1,x+1。根据题给条件可知,5x=85,则x=17,B为氯,A、C、D、E依次为F、S、Ar、Br。
但这五种元素的核外电子之和,也就是原子序数之和大于85,因此与题给条件不符。若A、B、E为ⅢA至ⅦA族元素,设B的原子序数为x,则A、E,C、D的原子序数依次为x—8,x+18,x—1,x+1,则5x+10=85,则x=15,B为磷,则A、C、D、E依次为N、Si、S、As元素,符合题意。故正确选项为A。 点评:本题考查的是原子结构与元素周期表中元素的位置的关系及周期表的结构。由题 给条件可知E是第四周期元素,且A、B、E处于周期表中同一主族。本题解题的关键是要掌握第四周期与第三周期同主族元素原子序数之差可能有两种情况:若是ⅠA、ⅡA族,则原子序数相差8;若是ⅢA~ⅦA及O族,则原子序数相差18。本题还可采用把选项代人验证的方法求解。
|

练习册系列答案
相关题目
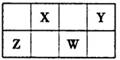
X、Y、Z、W均为短周期主族元素,下图为周期表的一部分。下列说法正确的是
| A.通常情况下,X元素只存在两种氧化物 |
| B.Y元素气态氢化物的还原性最强 |
| C.X元素的非金属性比Y元素非金属性强 |
| D.Z和X可能以共价键结合形成一种无机非金属材料 |