题目内容
短周期主族元素X、Y、Z、W,原子序数依次增大。X、Z同主族,X、Y、Z三种元素原子的最外层电子数之和为15,Y原子最外层电子数等于X原子最外层电子数的一半。下列叙述正确的是
A. 非金属性: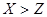
B. 原子半径: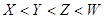
C. 最高价氧化物对应水化物的酸性: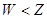
D. 单质Y常温下能溶于浓硝酸
【答案】
A
【解析】设Y原子最外层电子数为n,则X和Z原子最外层电子数都是2n,则有2n+n+2n=15,解得n=3,因此X是O,Y是Al,Z是S,W是Cl,所以A正确。同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,因此原子半径大小顺序为Y>Z>W>X,B不正确。非金属性越强,最高价氧化物的水合物的酸性越强,非金属性是Cl>S,因此高氯酸的酸性强于硫酸的,C不正确。常温下铝能和浓硝酸发生钝化,D不正确,答案选A。

练习册系列答案
相关题目
短周期主族元素X,Y,A,B,C在元素周期表的位置如图所示,A是电负性最大的元素,则下列说法不正确的是( )
| X | A | ||
| Y | C | B |
| A、原子半径由小到大的顺序为:A<B<C<Y |
| B、A、B的氢化物的沸点由低到高的顺序为:HA<HB |
| C、X、Y最高价氧化物对应的水化物的酸性由弱到强的顺序为:H2YO3<H2XO3 |
| D、B、C简单离子的还原性由弱到强的顺序为:B-<C 2- |
短周期主族元素X、Y、Z、W在元素周期表中的相对位置如表中所示.下列判断不正确的是( )
| Y | W | |
| X | Z |
| A、原子半径最大的是X |
| B、电负性最大的是W |
| C、Y、Z原子序数差为8 |
| D、氢化物最稳定的是Z |
 短周期主族元素X、Y、Z、W、M在元素周期表中的位置如图,W最高价氧化物对应的水化物为强酸,下列说法正确的是( )
短周期主族元素X、Y、Z、W、M在元素周期表中的位置如图,W最高价氧化物对应的水化物为强酸,下列说法正确的是( )| A、原子半径:Y<Z<M | B、M最高价氧化物对应的水化物一定是强酸 | C、Z与M对应的氢化物的沸点:M>Z | D、一定条件下,M、Y对应的单质都能与W的氢化物发生置换反应 |