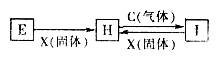题目内容
下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是
 物质 物质组别 | 甲 | 乙 | 丙 |
| A | Al | HCl | NaOH |
| B | NH3 | O2 | HNO3 |
| C | SiO2 | NaOH | HF |
| D | SO2 | Ca(OH)2 | NaHCO3 |
B
解析试题分析:A、铝与盐酸和氢氧化钠溶液均反应,盐酸与氢氧化钠也反应,A正确;B、氨气与氧气反应生成NO和水,氨气与硝酸反应生成硝酸铵,但氧气与硝酸不反应,B不正确;C、二氧化硅与氢氧化钠反应生成硅酸钠和水,与氢氟酸反应生成四氟化硅与水,氢氟酸与氢氧化钠发生中和反应,C正确;D、SO2与氢氧化钙反应生成亚硫酸钙和水,与碳酸氢钠反应生成CO2、水和亚硫酸钠,氢氧化钙与碳酸氢钠反应生成碳酸钙、碳酸钠和水或碳酸钙、氢氧化钠和水,D正确,答案选B。
考点:考查物质间反应的有关判断

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
下列根据实验事实得出的结论正确的是
| | 实 验 事 实 | 结 论 |
| A | 加热的铝箔熔化,但液态的铝不滴落 | 熔点:氧化铝>铝 |
| B | 溶液中加入盐酸酸化的BaCl2溶液有白色沉淀生成 | 该溶液中一定含有SO42- |
| C | 碳酸钠溶液能使酚酞试液变红 | 碳酸钠溶液呈碱性 |
| D | 常温下,铜与冷的浓H2SO4不反应 | 铜与浓硫酸发生钝化 |
金属材料在日常生活以及生产中有着广泛的运用。下列关于金属的一些说法不正确的是
| A.合金的性质与其成分金属的性质不完全相同 |
| B.工业上金属Mg、Al都是用电解熔融的氯化物制得的 |
| C.金属冶炼的本质是金属阳离子得到电子变成金属原子 |
| D.越活泼的金属越难冶炼 |
下列说法正确的是( )
| A.有些活泼金属如铝可用作热还原法的还原剂 |
| B.用电解NaCl溶液的方法来冶炼金属钠 |
| C.可用焦炭或一氧化碳还原氧化铝的方法来冶炼铝 |
| D.使元素由化合态转化成游离态的过程就是还原的过程 |
已知:2[NaAl(OH)4]+CO2→2Al(OH)3↓+Na2CO3+H2O。向含2molNaOH、1molBa(OH)2、2mol[NaAl(OH)4]的混合液中慢慢通入CO2,则通入CO2的量和生成沉淀的量的关系正确的是
| 选项 | A | B | C | D |
| n(CO2)(mol) | 2 | 3 | 4 | 6 |
| n(沉淀)(mol) | 1 | 2 | 3 | 3 |
中学化学中很多“规律”都有适用范围,下列根据有关“规律”推出的结论正确的是
| 选项 | 规律 | 结论 |
| A | 较强酸可以制取较弱酸 | 次氯酸溶液无法制取盐酸 |
| B | 反应物浓度越大,反应速率越快 | 常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 |
| C | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | NH3沸点低于PH3 |
| D | 溶解度小的沉淀易向溶解度更小的沉淀转化 | ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀 |
向100 mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2 mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如下图所示。下列判断正确的是( )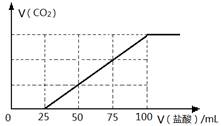
| A.原NaOH溶液的浓度为0.1 mol/L |
| B.通入CO2的体积为448 mL |
| C.所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na2CO3) =" 1:" 3 |
| D.所得溶液的溶质成分的物质的量之比为n(NaHCO3):n(Na2CO3) =" 2:" 1 |