题目内容
(2009?韶关一模)关于如图装置的叙述,正确的是( )
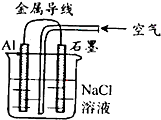

分析:该装置是原电池,铝作负极,石墨作正极,负极上铝失电子发生氧化反应生成铝离子,正极上氧气得电子发生还原反应生成氢氧根离子,铝离子和氢氧根离子反应生成难溶性的氢氧化铝.
解答:解:该装置是原电池,铝作负极,石墨作正极,
A.铝是负极,负极上铝失电子发生氧化反应生成铝离子,电极反应式为:Al-3e-=Al3+,故A错误;
B.石墨是正极,石墨上氧气得电子和水反应生成氢氧根离子,电极反应式为:2H2O+O2+4e-=4OH-,故B错误;
C.负极上的电极反应式为:Al-3e-=Al 3+,正极上的电极反应式为:2H2O+O2+4e-=4 OH-,铝离子和氢氧根离子反应生成难溶性的氢氧化铝,故C正确;
D.如果正负极上转移电子数相等,则n(Al3+):n( OH-)>1:4,所以不能最后完全沉淀溶解,故D错误;
故选C.
A.铝是负极,负极上铝失电子发生氧化反应生成铝离子,电极反应式为:Al-3e-=Al3+,故A错误;
B.石墨是正极,石墨上氧气得电子和水反应生成氢氧根离子,电极反应式为:2H2O+O2+4e-=4OH-,故B错误;
C.负极上的电极反应式为:Al-3e-=Al 3+,正极上的电极反应式为:2H2O+O2+4e-=4 OH-,铝离子和氢氧根离子反应生成难溶性的氢氧化铝,故C正确;
D.如果正负极上转移电子数相等,则n(Al3+):n( OH-)>1:4,所以不能最后完全沉淀溶解,故D错误;
故选C.
点评:本题考查原电池原理,明确正负极上发生的反应是解本题的关键,易错选项是D,根据铝离子和氢氧根离子的关系确定铝元素的存在形式,为易错点.

练习册系列答案
相关题目

 (2009?韶关一模)一定温度下,在密闭容器内进行着某一反应,X气体(2mol)、Y气体(10mol)的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
(2009?韶关一模)一定温度下,在密闭容器内进行着某一反应,X气体(2mol)、Y气体(10mol)的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )