题目内容
随着科学技术的进步,人们研制出了多种类型的甲醇质子交换膜燃料电池,以满足不同的需求.
(1)有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol
②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g)△H=-192.9kJ/mol
由上述方程式可知,CH3OH的燃烧热
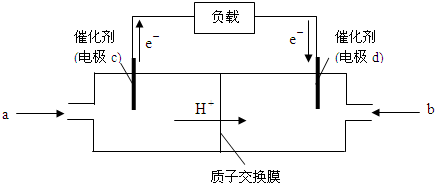
(2)下图是某笔记本电脑用甲醇质子交换膜燃料电池的结构示意图.甲醇在催化剂作用下提供质子和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O.则c电极是
(1)有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol
②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g)△H=-192.9kJ/mol
由上述方程式可知,CH3OH的燃烧热
大于
大于
(填“大于”、“等于”或“小于”)192.9kJ/mol.已知水的气化热为44kJ/mol,则氢气燃烧热的热化学方程式为H2(g)+
O2(g)=H2O(l)△H=-124.6kJ/mol
| 1 |
| 2 |
H2(g)+
O2(g)=H2O(l)△H=-124.6kJ/mol
.| 1 |
| 2 |
(2)下图是某笔记本电脑用甲醇质子交换膜燃料电池的结构示意图.甲醇在催化剂作用下提供质子和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O.则c电极是
负极
负极
(填“正极”或“负极”),c电极上发生的电极反应是CH3OH-6e-+H2O=CO2+6H+
CH3OH-6e-+H2O=CO2+6H+
.
分析:(1)燃烧热是指可燃物完全燃烧生成稳定的氧化物所放出的热量,应生成液态水,而气态水变为液态水要放出热量,可利用盖斯定律计算反应热;
(2)原电池中电子从负极经外电路流向正极,负极反应氧化反应.
(2)原电池中电子从负极经外电路流向正极,负极反应氧化反应.
解答:解:(1)燃烧热是指可燃物完全燃烧生成稳定的氧化物所放出的热量,应生成液态水,而气态水变为液态水要放出热量,由以上热化学方程式可以看出,当生成气态水时放出的热量为192.9kJ,则生成液态水应放出更多的热量,
已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol
②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g)△H=-192.9kJ/mol
利用盖斯定律将②-①可得:
O2(g)+3H2(g)=3H2O(g)△H=-241.9kJ/mol
即
O2(g)+H2(g)=H2O(g)△H=-80.6kJ/mol
又知:H2O(g)=H2O(l)△H=-44kJ/mol
则有:H2(g)+
O2(g)=H2O(l)△H=-(80.6+44)kJ/mol=-124.6kJ/mol,
故答案为:大于;H2(g)+
O2(g)=H2O(l)△H=-124.6kJ/mol;
(2)原电池中电子从负极经外电路流向正极,根据电子流向可知c电极为负极,
甲醇在负极上发生氧化反应,电极反应式为CH3OH-6e-+H2O=CO2+6H+,
故答案为:负极;CH3OH-6e-+H2O=CO2+6H+.
已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol
②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g)△H=-192.9kJ/mol
利用盖斯定律将②-①可得:
| 3 |
| 2 |
即
| 1 |
| 2 |
又知:H2O(g)=H2O(l)△H=-44kJ/mol
则有:H2(g)+
| 1 |
| 2 |
故答案为:大于;H2(g)+
| 1 |
| 2 |
(2)原电池中电子从负极经外电路流向正极,根据电子流向可知c电极为负极,
甲醇在负极上发生氧化反应,电极反应式为CH3OH-6e-+H2O=CO2+6H+,
故答案为:负极;CH3OH-6e-+H2O=CO2+6H+.
点评:本题考查化学反应与能量,题目难度中等,注意利用盖斯定律计算反应热.

练习册系列答案
相关题目
(共10分)
(1)已知可逆反应:M(g)+N(g) P(g)+Q(g);△H>0,请回答下列问题:
P(g)+Q(g);△H>0,请回答下列问题:
①若要增大M的转化率,在其它条件不变的情况下可以采取的措施为_______________。
| A.加入一定量M | B.加入一定量N |
| C.反应温度升高 | D.缩小容器体积 |
②在某温度下,反应物的起始浓度分别为:c(M)=" 1" mol·L-1,c(N)="2.4" mol·L-1,达到平衡后,M的转化率为60%,此时N的转化率为_______________。此反应的化学平衡常数K=_______________。
③若反应温度不变,反应物的起始浓度分别为:c(M)=" 4" mol·L-1,c(N)="a" mol·L-1;达到平衡后,c(P)="2" mol·L-1,a=_______________mol·L-1。
(2)随着科学技术的进步,人们研制出了多种类型的甲醇质子交换膜燃料电池,以满足不同的需求。
下图是某笔记本电脑用甲醇质子交换膜燃料电池的结构示意图。甲醇在催化剂作用下提供质子和电子(电子转移的方向如下图所示),电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH3OH+3O2===2CO2+4H2O。则c电极是 (填“正极”或“负极”),c电极上发生的电极反应式为_____________________________________________。

 (2011?湖南二模)(1)已知可逆反应:M(g)+N(g)
(2011?湖南二模)(1)已知可逆反应:M(g)+N(g) P(g)+Q(g);△H>0,请回答下列问题:
P(g)+Q(g);△H>0,请回答下列问题: P(g)+Q(g);△H>0,请回答下列问题:
P(g)+Q(g);△H>0,请回答下列问题: