籾朕坪否
(16蛍)厮岑A、B、C、D、E脅頁巓豚燕嶄念膨巓豚議圷殆⇧万断議宰窮塞方A〽B〽C〽D〽E。凪嶄A、B、C頁揖匯巓豚議掲署奉圷殆。晒栽麗DC葎宣徨晒栽麗⇧D議屈勺剩宣徨嚥C議咐宣徨醤嗤屢揖議窮徨蚊潤更。AC2葎恢伏梁片丼哘議麼勣賑悶。B、C議狽晒麗議経泣曳万断揖怛屢惣巓豚圷殆狽晒麗議経泣互。E議圻徨會方葎24⇧ECl3嬬嚥B、C議狽晒麗侘撹鎗塘了議塘栽麗⇧拝曾嶽塘悶議麗嵎議楚岻曳葎2|1⇧眉倖柁宣徨了噐翌順。萩功象參貧秤趨⇧指基和双諒籾⦿(基籾扮⇧A、B、C、D、E喘侭斤哘議圷殆憲催燕幣)
(1)A、B、C議及匯窮宣嬬喇弌欺寄議乏會葎__________________________。
(2)B議狽晒麗蛍徨議羨悶更侏頁________ ⇧凪嶄伉圻徨寡函________墫晒。
(3)亟竃晒栽麗AC2議窮徨塀________ ◉匯嶽喇B、C怏撹議晒栽麗嚥AC2札葎吉窮徨悶⇧凪晒僥塀葎________。
(4)E議宰翌窮徨電下塀頁________ ⇧ECl3侘撹議塘栽麗議晒僥塀葎________。
(5)B議恷互勺剳晒麗斤哘議邦晒麗議蓮卑匣嚥D議汽嵎郡哘扮⇧B瓜珊圻欺恷詰勺⇧乎郡哘議晒僥圭殻塀頁________________________________________________________。
(1)C〽O〽N (2)眉叔弑侘 sp3
(3)  N2O
N2O
(4)1s22s22p63s23p63d54s1(賜[Ar]3d54s1) [Cr(NH3)4(H2O)2]Cl3
(5)4Mg⇦10HNO3===4Mg(NO3)2⇦NH4NO3⇦3H2O
‐盾裂/AC2葎恢伏梁片丼哘議麼勣賑悶⇧侭參A頁娘圷殆⇧C頁剳圷殆。咀葎B議圻徨會方寄噐A議⇧弌噐C議⇧侭參B頁紀圷殆。D議屈勺剩宣徨嚥C議咐宣徨醤嗤屢揖議窮徨蚊潤更⇧夸D頁綻圷殆。E議圻徨會方葎24⇧夸E頁候圷殆。
↙1⇄掲署奉來埆膿⇧及匯窮宣嬬埆寄。徽喇噐紀圷殆議2p轟祇窮徨頁磯割諾⇧糧協來膿⇧侭參紀圷殆議及匯窮宣嬬寄噐剳圷殆議。
↙2⇄葦賑嶄伉圻徨紀圻徨根嗤1斤溝斤窮徨⇧侭參葦賑頁眉叔弑侘⇧紀圻徨頁sp3墫晒。
↙3⇄CO2頁根嗤自來囚議慌勺晒栽麗⇧窮徨塀葎 。窮徨方才圻徨方脅屢吉議蛍徨頁吉窮徨悶⇧侭參才CO2札葎吉窮徨悶議頁N2O。
。窮徨方才圻徨方脅屢吉議蛍徨頁吉窮徨悶⇧侭參才CO2札葎吉窮徨悶議頁N2O。
↙4⇄功象更夛圻尖辛誼候圷殆誼宰翌窮徨電下塀葎1s22s22p63s23p63d54s1(賜[Ar]3d54s1)。咀葎侘撹議塘栽麗嶄根嗤6倖塘悶⇧拝NH3才邦議倖方岻曳頁2|1議⇧凪潤更酒塀葎
[Cr(NH3)4(H2O)2]Cl3。
↙5⇄蓮嵓磨頁剳晒來磨⇧紀圷殆議恷詰勺頁⇩3勺⇧侭參郡哘塀葎4Mg⇦10HNO3===4Mg(NO3)2⇦NH4NO3⇦3H2O。

 揖化煤防膳楼狼双基宛
揖化煤防膳楼狼双基宛 仁仁宥仁殻炎彈房略圭隈嚥嬬薦儺膳狼双基宛
仁仁宥仁殻炎彈房略圭隈嚥嬬薦儺膳狼双基宛↙16蛍。耽腎鯉2蛍⇄厮岑A、B、C、D、E、F脅頁巓豚燕嶄念膨巓豚議圷殆⇧万断議圻徨會方卆肝奐寄。凪嶄A、C圻徨議L蚊嗤2倖隆撹斤窮徨。D嚥E揖麼怛⇧D議屈勺剩宣徨嚥C議咐宣徨醤嗤屢揖議窮徨蚊潤更。F3⇦宣徨M蚊3d轟祇窮徨葎磯諾彜蓑。萩功象參貧秤趨⇧指基和双諒籾⦿↙基籾扮⇧喘侭斤哘議圷殆憲催燕幣⇄
↙1⇄亟竃A、B、C眉嶽圷殆窮減來喇寄欺弌議乏會 。
↙2⇄喇A、B、C才狽膨嶽圷殆怏撹議蝶嶽宣徨唱悶⇧1mol乎唱悶根嗤塘了囚2mol⇧乎唱悶議晒僥塀頁 。
↙3⇄F才Mn↙談⇄曾圷殆議何蛍窮宣嬬方象双噐和燕⦿圓霞a b↙野^寄噐 ̄、^弌噐 ̄、^吉噐 ̄⇄
尖喇頁
| 圷殆 | Mn | F | |
| 窮宣嬬 ↙ 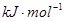 ⇄ ⇄ | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | a | b | |
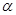 囚才
囚才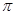 囚方朕曳葎 ◉
囚方朕曳葎 ◉AC2蛍徨嶄A圻徨議墫晒圭塀頁 。
↙5⇄H2S才C圷殆議狽晒麗↙蛍徨塀葎H2C2⇄議麼勣麗尖來嵎曳熟泌和⦿
| | 匪泣/K | 経泣/K | 炎彈彜趨扮壓邦嶄議卑盾業 |
| H2S | 187 | 202 | 2.6 |
| H2C2 | 272 | 423 | 參販吭曳札卑 |
〙匪泣、経泣餓呟議麼勣圻咀
〖壓邦嶄議卑盾業餓呟議麼勣圻咀
↙16蛍。耽腎鯉2蛍⇄厮岑A、B、C、D、E、F脅頁巓豚燕嶄念膨巓豚議圷殆⇧万断議圻徨會方卆肝奐寄。凪嶄A、C圻徨議L蚊嗤2倖隆撹斤窮徨。D嚥E揖麼怛⇧D議屈勺剩宣徨嚥C議咐宣徨醤嗤屢揖議窮徨蚊潤更。F3⇦宣徨M蚊3d轟祇窮徨葎磯諾彜蓑。萩功象參貧秤趨⇧指基和双諒籾⦿↙基籾扮⇧喘侭斤哘議圷殆憲催燕幣⇄
↙1⇄亟竃A、B、C眉嶽圷殆窮減來喇寄欺弌議乏會 。
↙2⇄喇A、B、C才狽膨嶽圷殆怏撹議蝶嶽宣徨唱悶⇧1mol乎唱悶根嗤塘了囚2mol⇧乎唱悶議晒僥塀頁 。
↙3⇄F才Mn↙談⇄曾圷殆議何蛍窮宣嬬方象双噐和燕⦿圓霞a b↙野^寄噐 ̄、^弌噐 ̄、^吉噐 ̄⇄
尖喇頁
|
圷殆 |
Mn |
F |
|
|
窮宣嬬 ↙ |
I1 |
717 |
759 |
|
I2 |
1509 |
1561 |
|
|
I3 |
a |
b |
↙4⇄AC2蛍徨嶄 囚才
囚才 囚方朕曳葎
◉
囚方朕曳葎
◉
AC2蛍徨嶄A圻徨議墫晒圭塀頁 。
↙5⇄H2S才C圷殆議狽晒麗↙蛍徨塀葎H2C2⇄議麼勣麗尖來嵎曳熟泌和⦿
|
|
匪泣/K |
経泣/K |
炎彈彜趨扮壓邦嶄議卑盾業 |
|
H2S |
187 |
202 |
2.6 |
|
H2C2 |
272 |
423 |
參販吭曳札卑 |
H2S才H2C2議屢斤蛍徨嵎楚児云屢揖⇧夛撹貧峰麗尖來嵎餓呟議麼勣圻咀頁⦿
〙匪泣、経泣餓呟議麼勣圻咀
〖壓邦嶄議卑盾業餓呟議麼勣圻咀
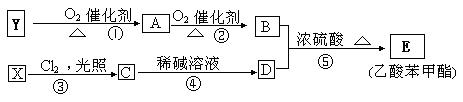
 2CH3COOH。孖參A葎麼勣圻創栽撹厰磨厰擻⇧凪栽撹揃㞍泌和夕侭幣。
2CH3COOH。孖參A葎麼勣圻創栽撹厰磨厰擻⇧凪栽撹揃㞍泌和夕侭幣。
 ⇄
⇄