题目内容
(1)计算273 K、101.325 kPa下,1 mol冰融化时的熵变ΔS(冰的融化热为ΔH=6 000 J·mol-1)。(2)高温时空气中的N2和O2会反应生成NO而污染大气:N2(g)+O2(g)![]() 2NO(g)。试通过计算说明在1
2NO(g)。试通过计算说明在1
解析:(1)H2O(s)![]() H2O(l),是一个平衡状态,ΔH-TΔS=0,ΔH=6 000 J·mol-1,ΔS=
H2O(l),是一个平衡状态,ΔH-TΔS=0,ΔH=6 000 J·mol-1,ΔS=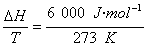 =22.0 J·mol-1·K-1。?
=22.0 J·mol-1·K-1。?
(2)ΔH-TΔS=180.50 kJ·mol-1-1 473 K×0.024 77 kJ·mol-1·K-1=144.01 kJ·mol-1>0,正反应不能自发进行。根据平衡状态时ΔH-TΔS=0,求自发进行的最低温度(即转化温度),T=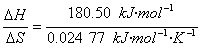 =7 287 K,即此反应自发进行的最低温度是7 287 K。?
=7 287 K,即此反应自发进行的最低温度是7 287 K。?
答案:(1)22.0 J·mol-1·K-1?
(2)不能自发进行,自发进行的最低温度为7 287 K。?

练习册系列答案
相关题目
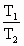 =
=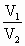 [式中T指绝对温标,T(K)=273+t C]
[式中T指绝对温标,T(K)=273+t C]