��Ŀ����
����Ŀ����֪25��ʱ��Ksp[Mg(OH)2] =5.61��l0-12��Ksp[Al(OH)3] =1.3��l0-33��Al(OH)3![]() AlO2-+H++H2O Ka=6.31��l0-13��ij��Һ�п��ܺ��� H+��Na+��Mg2+��Al3+��Cl-��HCO3-�����ӡ������Һ�м���һ�����ʵ���Ũ�ȵ�NaOH��Һʱ���������ɳ��������ʵ�����NaOH��Һ������仯��ͼ��ʾ�������й�˵����ȷ����
AlO2-+H++H2O Ka=6.31��l0-13��ij��Һ�п��ܺ��� H+��Na+��Mg2+��Al3+��Cl-��HCO3-�����ӡ������Һ�м���һ�����ʵ���Ũ�ȵ�NaOH��Һʱ���������ɳ��������ʵ�����NaOH��Һ������仯��ͼ��ʾ�������й�˵����ȷ����

A. b �������Al(OH)3��d �������A1(OH)3��Mg(OH)2��e�����ʡ�NaA1O2
B. �������⣬��NaOH������ȫ����Mg2+��Al3+����
C. cd �η����ķ�ӦΪ��Mg2+ +2OH- =Mg(OH)2��
D. bc �η����ķ�ӦΪ:Al(OH)3+OH-=A1O2-+2H2O
���𰸡�D
������������ͼ���һ�Σ������������ϳ��֣���֪һ���������ӣ�����кͷ�Ӧ��һ�з�Ӧ�����ȷ�Ӧ����һ��������HCO3-��������ֻ����Cl-��������֪25��ʱ��Ksp[Mg(OH)2] =5.61��l0-12��Ksp[Al(OH)3] =1.3��l0-33��Al(OH)3![]() AlO2-+H++H2O Ka=6.31��l0-13��ab������������ʼ������þ���ӻ�û��ʼ������bc������������ʼ�ܽ⣬ cd���������������ܽⲢ����������þ���ҳ������ӣ�d��������þ�����ﵽ����������������������ܽ⣬e�����������ܽ���ȫ����A��b �������Al(OH)3��d �������Mg(OH)2��e�����ʡ�NaA1O2��NaCl��ѡ��A����B����NaOH����e�����ȫ����Mg2+��Al3+��ѡ��B����C��cd �η����ķ�ӦΪ��Mg2+ +2OH-=Mg(OH)2����Al(OH)3+OH-=A1O2-+2H2O��ѡ��C����D��bc �η����ķ�ӦΪ:Al(OH)3+OH-=A1O2-+2H2O��ѡ��D��ȷ����ѡD��
AlO2-+H++H2O Ka=6.31��l0-13��ab������������ʼ������þ���ӻ�û��ʼ������bc������������ʼ�ܽ⣬ cd���������������ܽⲢ����������þ���ҳ������ӣ�d��������þ�����ﵽ����������������������ܽ⣬e�����������ܽ���ȫ����A��b �������Al(OH)3��d �������Mg(OH)2��e�����ʡ�NaA1O2��NaCl��ѡ��A����B����NaOH����e�����ȫ����Mg2+��Al3+��ѡ��B����C��cd �η����ķ�ӦΪ��Mg2+ +2OH-=Mg(OH)2����Al(OH)3+OH-=A1O2-+2H2O��ѡ��C����D��bc �η����ķ�ӦΪ:Al(OH)3+OH-=A1O2-+2H2O��ѡ��D��ȷ����ѡD��

 �Ķ��쳵ϵ�д�
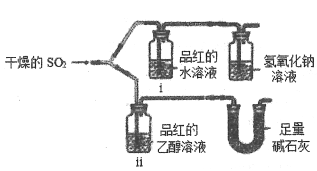
�Ķ��쳵ϵ�д�����Ŀ����ʢ��H2O2��Һ���Թ��е�������Ũ���ᣬ���������ɵĻ��������ֻ����O2��Cl2��HCl��ˮ������������ͨ��X��Һ����ͼ�������ݹ۲쵽���������ж������к���Cl2���ǣ� ��
ѡ�� | X��Һ | ���� |
|
A | ϡHNO3�ữ��AgNO3��Һ | �а�ɫ�������� | |
B | ����KSCN��FeSO4��Һ | ��Һ��ΪѪ��ɫ | |
C | ����KI������Һ | ��Һ��Ϊ��ɫ | |
D | ��ɫʯ����Һ | ��Һ�ȱ�����ɫ |
A. A B. B C. C D. D