题目内容
下列实验不能达到预期目的是( )


| A、图Ⅰ用于稀释浓硫酸 |
| B、利用Ⅱ装置制取C2H4 |
| C、利用Ⅲ装置进行铜与浓硝酸反应的实验 |
| D、利用Ⅳ装置收集NH3 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.不能在容量瓶中稀释浓硫酸;
B.温度计应插入到液面以下;
C.浓硝酸和铜反应生成二氧化氮,用氢氧化钠溶液吸收;
D.氨气密度比空气小,用向下排空法收集,易溶于水.
B.温度计应插入到液面以下;
C.浓硝酸和铜反应生成二氧化氮,用氢氧化钠溶液吸收;
D.氨气密度比空气小,用向下排空法收集,易溶于水.
解答:
解:A.容量瓶只能在常温下使用,不能在容量瓶中稀释浓硫酸,故A错误;
B.利用Ⅱ装置制取C2H4,应加热到170℃,温度计应插入到液面以下,故B错误;
C.浓硝酸和铜反应生成二氧化氮,可用氢氧化钠溶液吸收,防止污染空气,故C正确;
D.氨气密度比空气小,用向下排空法收集,易溶于水,装置可防止倒吸,故D正确.
故选AB.
B.利用Ⅱ装置制取C2H4,应加热到170℃,温度计应插入到液面以下,故B错误;
C.浓硝酸和铜反应生成二氧化氮,可用氢氧化钠溶液吸收,防止污染空气,故C正确;
D.氨气密度比空气小,用向下排空法收集,易溶于水,装置可防止倒吸,故D正确.
故选AB.
点评:本题考查化学实验方案的评价,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质以及实验方案的严密性、可行性的评价,难度不大.

练习册系列答案
相关题目
pH值相同的盐酸和醋酸两种溶液中,它们的( )
| A、H+的物质的量相同 |
| B、盐酸和醋酸的物质的量浓度相同 |
| C、H+的物质的量浓度不同 |
| D、OH-的物质的量浓度相同 |
下列叙述正确的是( )
| A、摩尔是物质的量的单位,简称摩,符号为mol |
| B、CH4的摩尔质量为16 |
| C、2mol HCl溶于1L水所得盐酸物质的量为2mol/L |
| D、1mol任何气体的体积都约为22.4L |
 W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )| A、X、Y、Z中最简单氢化物稳定性最弱的是Z |
| B、Z和Y元素的氧化物对应水化物的酸性Z一定强于Y |
| C、简单阴离子的还原性:X<Y |
| D、最简单氢化物的沸点:X<Y |
分类方法在化学学科的发展中起到非常重要的作用.下列分类标准合理的是①根据酸分子中含有氢原子的个数,将酸分为一元酸、二元酸、三元酸等②根据化合物在溶液中电离出离子的类别,将化合物分为酸、碱、盐
③根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液④根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应( )
③根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液④根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应( )
| A、①③ | B、②③④ |
| C、①②④ | D、②④ |
相同物质的量的下列有机物,充分燃烧,消耗氧气量相同的是( )
| A、C3H4和C2H6 |
| B、C3H6和C3H8O |
| C、C3H6O2和C3H8O |
| D、C3H8O和C4H8O2 |
 短周期元素X、Y、Z、W在元素周期表中的位置如图所示,Z原子最外层电子数是其电子层数的2倍,下列叙述正确的是( )
短周期元素X、Y、Z、W在元素周期表中的位置如图所示,Z原子最外层电子数是其电子层数的2倍,下列叙述正确的是( )| A、原子半径的大小顺序为:rZ>rW>rX>rY |
| B、元素W的含氧酸的酸性一定比Z的含氧酸的酸性强 |
| C、工业上是通过电解法获得元素W的单质 |
| D、XZ2和XW4中化学键的类型不同 |
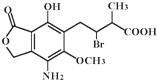 某有机物A的结构简式如图,下列有关A的说法正确的是( )
某有机物A的结构简式如图,下列有关A的说法正确的是( )| A、分子式为:C14H25O6NBr |
| B、该有机物能发生水解反应,但不能发生消去反应 |
| C、该有机物能使酸性高锰酸钾溶液褪色 |
| D、A在一定条件下与氢氧化钠溶液反应,1 molA最多消耗4mol NaOH |