题目内容
4.下列事实不能说明元素的金属性或非金属性相对减弱的是( )| 序号 | 事实 | 推论 |
| A | Ca(OH)2的碱性强于Mg(OH)2 | 金属性:Ca>Mg |
| B | 与冷水反应,Na比Mg剧烈 | 金属性:Na>Mg |
| C | SO2与NaHCO3溶液反应生成CO2 | 非金属性:S>C |
| D | t℃时,Br2+H2?2HBr K=5.6×107 I2+H2?2HI K=43 | 非金属性:Br>I |
| A. | A | B. | B | C. | C | D. | D |
分析 A.金属性越强,对应的最高价氧化物的水化物碱性越强;
B.金属性越强,与水反应越剧烈;
C.SO2与NaHCO3溶液反应生成CO2,可知酸性亚硫酸大于碳酸;
D.K越大,说明生成的气态氢化物越稳定.
解答 解:A.Ca、Mg位于同主族,金属性Ca>Mg,对应的最高价氧化物的水化物碱性为Ca(OH)2强于Mg(OH)2,故A正确;
B.Na、Mg位于同周期,金属性Na>Mg,则与冷水反应,Na比Mg剧烈,故B正确;
C.SO2与NaHCO3溶液反应生成CO2,可知酸性亚硫酸大于碳酸,亚硫酸不是最高价氧化物的水化物,则不能以此比较非金属性,故C错误;
D.K越大,说明生成的气态氢化物越稳定,则稳定性为HBr>HI,则非金属性为Br>I,故D正确;
故选C.
点评 本题考查金属性及非金属性的比较,为高频考点,把握元素的位置、元素周期律及比较方法为解答的关键,注意归纳金属性、非金属性比较方法,题目难度不大,选项C为易错点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.在一定条件下,将3molA和1molB两种其他混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)═xC(g)+2D(s).2min 时该反应达到平衡,生成了0.8molD,并测得C的浓度为0.2mol•L-1.下列判断错误的是( )
| A. | x=1 | |
| B. | 充入稀有气体增大体系压强,可提高该反应的反应速率 | |
| C. | 平衡时A与B的转化率相等,均为40% | |
| D. | 平衡时B与C的浓度之比为3:2 |
12.设NA代表阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 2.3g钠与水反应失去的电子数目为0.2NA | |
| B. | 20℃、101Kpa时,5.6L氨气所含的原子数目为NA | |
| C. | 0℃、101Kpa时,18g铵根离子所含有的电子数为10NA | |
| D. | 1mol氯化钠固体溶于1L水所得的溶液中氯化钠的物质的量浓度为1mol/L |
19.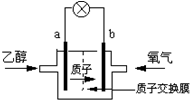 美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200℃时供电,乙醇电池比甲醇电池效率高出32倍且更安全.电池总反应为:C2H5OH+3O2═2CO2+3H2O,电池示意如图,下列说法不正确的是( )
美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200℃时供电,乙醇电池比甲醇电池效率高出32倍且更安全.电池总反应为:C2H5OH+3O2═2CO2+3H2O,电池示意如图,下列说法不正确的是( )
 美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200℃时供电,乙醇电池比甲醇电池效率高出32倍且更安全.电池总反应为:C2H5OH+3O2═2CO2+3H2O,电池示意如图,下列说法不正确的是( )
美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200℃时供电,乙醇电池比甲醇电池效率高出32倍且更安全.电池总反应为:C2H5OH+3O2═2CO2+3H2O,电池示意如图,下列说法不正确的是( )| A. | a极为电池的负极 | |
| B. | 电池工作时电流由b极沿导线经灯泡再到a极 | |
| C. | 电池正极的电极反应为:2H++O2+4e-═H2O | |
| D. | 电池工作时1mol乙醇被氧化时就有6mol电子转移 |
9.一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO12.0g,若上述气体为NO和NO2的混合物,且体积比为1﹕1,则V可能为( )
| A. | 13.5L | B. | 9.0L | C. | 16.8L | D. | 15.7L |
16.两个不同容积的容器中分别盛有H2、O2,已知两个容器中气体的温度、密度都相等,下列说法一定正确的是( )
| A. | 两种气体质量相等 | B. | 两种气体的物质的量之比为16:1 | ||
| C. | 两种气体压强比为16:1 | D. | 两种气体体积比为1:16 |
13.在下列物质:A.烧碱 B.硫酸 C.干冰 D.硫酸钡 E.纯碱 F.铁
(1)既不是电解质,也不是非电解质的是F(或铁).
(2)纯碱的电离方程式是Na2CO3=2Na++CO32-.
(3)烧碱溶液与稀硫酸混合,发生反应的离子方程式为H++OH-=H2O.
(4)将干冰升华后所得的气体通入过量烧碱溶液中,发生反应的离子方程式为
CO2+2OH-=CO32-+H2O.
(5)a、b、c、d是Na2CO3、BaCl2、HCl、AgNO3四种溶液中的一种,现将它们两两混合,现象如下表所示:
①b是HCl(用化学式填写).
②写出a+c反应的离子方程式Ag++Cl-=AgCl↓.
盐酸分子式:HCl相对分子质量:36.5密度:1.19g/cm3质量分数:36.5%
(1)既不是电解质,也不是非电解质的是F(或铁).
(2)纯碱的电离方程式是Na2CO3=2Na++CO32-.
(3)烧碱溶液与稀硫酸混合,发生反应的离子方程式为H++OH-=H2O.
(4)将干冰升华后所得的气体通入过量烧碱溶液中,发生反应的离子方程式为
CO2+2OH-=CO32-+H2O.
(5)a、b、c、d是Na2CO3、BaCl2、HCl、AgNO3四种溶液中的一种,现将它们两两混合,现象如下表所示:
| 反应物 | a+b | c+d | a+d | a+c | b+d |
| 现象 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 无色气体 |
②写出a+c反应的离子方程式Ag++Cl-=AgCl↓.
盐酸分子式:HCl相对分子质量:36.5密度:1.19g/cm3质量分数:36.5%
14.关于钠元素的单质及其化合物的叙述正确的是( )
| A. | 用洁净的铂丝蘸取样品在无色火焰上灼烧看见黄色火焰,说明样品中不含钾元素 | |
| B. | 钠可从硫酸铜溶液中置换出铜 | |
| C. | Na2O和Na2O2都是碱性氧化物 | |
| D. | Na2O2中阴离子的摩尔质量是32g•mol-1 |