题目内容
向浓度相等、体积均为50mL的A、B两份氢氧化钠溶液中分别通入一定量的二氧化碳后,再稀释至100mL。(1)向氢氧化钠溶液中通入一定量的二氧化碳后,溶液中溶质的可能组成有:①______;②_______;③_______;④_______。
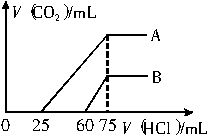
(2)向稀释后的溶液中逐滴加入0.1mol/L的盐酸溶液,产生二氧化碳的体积(标准状况)与所加盐酸溶液的体积关系如图所示。
①A曲线表明,向原溶液中通入二氧化碳后,所得溶质与HCl反应产生二氧化碳的最大体积是_______mL(标准状况)。
②B曲线表明,向原溶液中通入二氧化碳后,所得溶液中溶质的化学式为___________。
③原氢氧化钠溶液中NaOH的物质的量浓度为__________。
(1)①NaOH、Na2CO3 ②Na2CO3、NaHCO3 ③NaHCO3 ④Na2CO3
(2)①112 ②NaOH、Na2CO3 ③0.15mol/L
【试题分析】
本题考查同学们对多步反应与图像相结合试题的理解能力。
(1)根据化学方程式:2NaOH+CO2=Na2CO3+H2O、NaOH+CO2=NaHCO3知,溶液中溶质的可能组合方式有:①NaOH、Na2CO3;②Na2CO3、NaHCO3;③NaHCO3;④Na2CO3。
(2)题目中“逐滴”的含义是HCl依次发生下列反应:NaOH+HCl=NaCl+H2O、Na2CO3+HCl=NaCl+NaHCO3(不产生二氧化碳)、NaHCO3+HCl=NaCl+CO2↑+H2O(开始产生二氧化碳)。
根据开始产生二氧化碳时消耗盐酸溶液的量与产生二氧化碳最大量时消耗盐酸溶液的量的比值,讨论A溶液中溶质的成分。若A溶液中溶质为NaOH、Na2CO3,产生二氧化碳以前发生反应:NaOH+HCl=NaCl+H2O、Na2CO3+HCl=NaCl+NaHCO3;开始产生二氧化碳时发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O。前后两段消耗盐酸溶液的体积比大于1∶1。若A溶液中溶质为Na2CO3,则前后两段消耗盐酸溶液的体积比为1∶1。若A溶液中溶质为Na2CO3、NaHCO3,则前后两段消耗盐酸溶液的体积比小于1∶1。
①A曲线:开始滴加盐酸溶液至25mL时没有气体产生,滴加至75mL时碳酸盐完全反应,即生成二氧化碳达到最大值(不考虑溶液中溶解的二氧化碳)。前后两段消耗盐酸溶液的体积比为25∶50=1∶2<1∶1,故A溶液中溶质为Na2CO3、NaHCO3,且n(Na2CO3)∶n(NaHCO3)=1∶1。根据钠元素守恒知,当二氧化碳恰好达到最大值时,原溶液中钠离子全部以氯化钠存在。开始产生二氧化碳时一定是碳酸氢钠与盐酸反应,与碳酸氢钠反应的盐酸溶液为75mL-25mL=50mL。n(HCl)=50×10-3L×0.1mol/L=5×10-3mol,由化学方程式知,n(CO2)=5×10-3mol,V(CO2)=5×10-3mol×22.4L/mol=112mL。
②B曲线:产生二氧化碳前消耗盐酸溶液60mL,与碳酸氢钠反应消耗盐酸溶液15mL。前后两段消耗盐酸溶液的体积比为60∶15=4∶1,根据上述分析,可推知B溶液中的溶质为NaOH、Na2CO3。
③当加入盐酸溶液为75mL时,氢氧化钠全部转化成氯化钠。根据NaOH~NaCl~HCl知,n(NaOH)=n(HCl)=75×10-3L×0.1mol/L=7.5×10-3mol,c(NaOH)=7.5×10-3mol/0.05L=0.15mol/L。

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
 如图,有甲、乙两容器,甲体积可变,压强不变,乙保持体积不变.向两容器中分别充入1mol A,3mol B,此时两容器体积均为0.5L,温度为T℃,保持温度不变发生反应:A(g)+3B(g)?xC(g)+2D(s),乙容器中反应经4min后测得n(A)=0.5mol,v(c)=0.5mol?L-1?min-1.
如图,有甲、乙两容器,甲体积可变,压强不变,乙保持体积不变.向两容器中分别充入1mol A,3mol B,此时两容器体积均为0.5L,温度为T℃,保持温度不变发生反应:A(g)+3B(g)?xC(g)+2D(s),乙容器中反应经4min后测得n(A)=0.5mol,v(c)=0.5mol?L-1?min-1.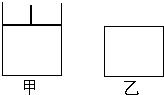 如图,有甲、乙两容器,甲体积可变压强不变,乙保持体积不变.向两容器中分别充入1molA、3molB,此时两容器体积均为500mL,温度为T℃.保持温度不变发生反应:
如图,有甲、乙两容器,甲体积可变压强不变,乙保持体积不变.向两容器中分别充入1molA、3molB,此时两容器体积均为500mL,温度为T℃.保持温度不变发生反应: 按要求填写下列空白.
按要求填写下列空白.