题目内容
1.A的产量可以用来衡量一个国家的石油化工发展水平.其与水加成的产物B是一种常用的有机溶剂,在生活中有重要的应用.①B的分子式为C2H6O.
②写出由A生成B的化学反应方程式:CH2═CH2+H-OH$→_{加热、加热}^{催化剂}$CH3-CH2-OH,其反应类型为加成反应.
分析 乙烯的产量可以用来衡量一个国家的石油化工发展水平,所以A为CH2═CH2,CH2═CH2和水发生加成反应生成B为CH3CH2OH,CH3CH2OH是一种常用的有机溶剂,在生活中有重要的应用.
解答 解:乙烯的产量可以用来衡量一个国家的石油化工发展水平,所以A为CH2═CH2,CH2═CH2和水发生加成反应生成B为CH3CH2OH,CH3CH2OH是一种常用的有机溶剂,在生活中有重要的应用,
①B为CH3CH2OH,B的分子式为C2H6O,
故答案为:C2H6O;
②CH2═CH2和水发生加成反应生成CH3CH2OH,反应的化学反应方程式为CH2═CH2+H-OH$→_{加热、加热}^{催化剂}$CH3-CH2-OH,反应类型为加成反应,
故答案为:CH2═CH2+H-OH$→_{加热、加热}^{催化剂}$CH3-CH2-OH;加成反应.
点评 本题考查了乙烯的化学性质、烷烃的结构等知识,难度不大,重点掌握稀的加成反应.

练习册系列答案
相关题目
12.某烃的结构简式为 ,它可能具有的性质是( )
,它可能具有的性质是( )
 ,它可能具有的性质是( )
,它可能具有的性质是( )| A. | 易溶于水,也易溶于有机溶剂 | |
| B. | 1 mol该烃含有4 mol碳碳双键 | |
| C. | 能发生聚合反应,其产物可表示为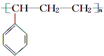 | |
| D. | 既能使溴水褪色,又能使酸性KMnO4溶液褪色 |
9.可以用浓磷酸代替浓硫酸制取溴化氢气体的理由是( )
| A. | 浓磷酸与浓硫酸的性质相似 | |
| B. | 浓磷酸与浓硫酸一样难挥发,且属非氧化性酸 | |
| C. | 浓磷酸无氧化性,只有还原性 | |
| D. | 浓磷酸的酸性强于氢溴酸 |
16.下列物质中,发生消去反应生成的烯烃只有一种的是( )
①2丁醇
②2甲基2丙醇
③1丁醇
④2甲基2丁醇.
①2丁醇
②2甲基2丙醇
③1丁醇
④2甲基2丁醇.
| A. | ①② | B. | ②③ | C. | ②④ | D. | ③④ |
13.下列比较不正确的是( )
| A. | 非金属性:C>N | B. | 酸性:HClO4>H2CO3 | ||
| C. | 碱性:NaOH>Mg(OH)2 | D. | 热稳定性H2O>H2S |
10.下列食物中属于酸性食物的是( )
| A. | 西红柿 | B. | 羊肉 | C. | 柠檬 | D. | 黄瓜 |
 ,它们的单质都必须采用电解法制备,但都无需密封保存,
,它们的单质都必须采用电解法制备,但都无需密封保存, .(2)Y元素在周期表中位置第三周期ⅢA族.
.(2)Y元素在周期表中位置第三周期ⅢA族. ,X、Y的最高价含氧酸的浓溶液都有强氧化性.
,X、Y的最高价含氧酸的浓溶液都有强氧化性.