题目内容
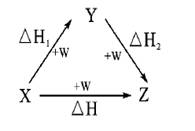
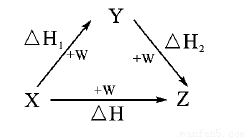
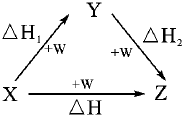
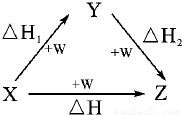
 符合如图所示的转化关系,且当X、Y、Z的物质的量相等时,存在焓变△H=△H1+△H2满足上述条件的X、Y可能是( )
符合如图所示的转化关系,且当X、Y、Z的物质的量相等时,存在焓变△H=△H1+△H2满足上述条件的X、Y可能是( )①C、CO②S、SO2③Na、Na2O④AlCl3、Al(OH)3⑤Fe、Fe(NO3)2⑥NaOH、Na2CO3.
分析:由盖斯定律可知,化学反应一步完成和分步完成,反应的焓变是相同的,然后利用发生的化学反应来分析焓变的关系,注意X、Y、Z的物质的量相等.
解答:解:①由C+O2
CO2,可看成C+
O2
CO、CO+
O2
CO2来完成,X、Y、Z的物质的量相等,符合△H=△H1+△H2,故①正确;
②因S与氧气反应生成二氧化硫,不会直接生成三氧化硫,则不符合转化,故②错误;
③由2Na+O2
Na2O2,可看成2Na+
O2═Na2O、Na2O+
O2═Na2O2来完成,X、Y、Z的物质的量相等时,不符合△H=△H1+△H2,故③错误;
④由AlCl3+4NaOH═3NaCl+NaAlO2+2H2O,可看成AlCl3+3NaOH═Al(OH)3↓+3NaCl、Al(OH)3+NaOH═NaCl+NaAlO2+2H2O来完成,X、Y、Z的物质的量相等,符合△H=△H1+△H2,故④正确;
⑤由Fe+4HNO3═Fe(NO3)3+NO↑+2H2O,可看成Fe+
HNO3═Fe(NO3)2+
NO↑+
H2O、Fe(NO3)2+
HNO3═Fe(NO3)3+
NO↑+
H2O来完成,X、Y、Z的物质的量相等,符合△H=△H1+△H2,故⑤正确;
⑥由NaOH+CO2═NaHCO3,可看成NaOH+
CO2═
Na2CO3+
H2O、
CO2+
Na2CO3+
H2O═NaHCO3,X、Z的物质的量相等,而Y的物质的量为X一半,不符合题意,故⑥错误;
故选A.
| ||
| 1 |
| 2 |
| ||
| 1 |
| 2 |
| ||
②因S与氧气反应生成二氧化硫,不会直接生成三氧化硫,则不符合转化,故②错误;
③由2Na+O2
| ||
| 1 |
| 2 |
| 1 |
| 2 |
④由AlCl3+4NaOH═3NaCl+NaAlO2+2H2O,可看成AlCl3+3NaOH═Al(OH)3↓+3NaCl、Al(OH)3+NaOH═NaCl+NaAlO2+2H2O来完成,X、Y、Z的物质的量相等,符合△H=△H1+△H2,故④正确;
⑤由Fe+4HNO3═Fe(NO3)3+NO↑+2H2O,可看成Fe+
| 8 |
| 3 |
| 2 |
| 3 |
| 4 |
| 3 |
| 4 |
| 3 |
| 1 |
| 3 |
| 2 |
| 3 |
⑥由NaOH+CO2═NaHCO3,可看成NaOH+
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
故选A.
点评:本题考查学生利用盖斯定律来分析焓变的关系,明确一步完成的反应可由哪些反应分步来完成及物质的物质的量的关系是解答本题的关键.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目