��Ŀ����
ʹһ��������п��100 mL��18.5 mol��L��1Ũ�����ַ�Ӧ��
(1)��п��ȫ�ܽ⣬ͬʱ���ɱ�״����SO2����3.36 L����������Һ������п�����ʵ���Ũ��(���跴Ӧǰ����Һ������ֲ���)��
(2)��п��ȫ�ܽ⣬ͬʱ���ɱ�״���»������Ϊ33.6 L��������Ӧ�����Һϡ����1 L�������Һ��c(H+)Ϊ0.100 mol��L��1�����������и���ֵ�����ȣ�
������
|
�������(1)Zn��2H2SO4(Ũ) ������������������������������1 mol������22.4 L ������������������������������n(ZnSO4)����3.36 L ������n(ZnSO4)��0.150 mol��c(ZnSO4)��1.50 mol��L��1�� ����(2)�����⣺��Ӧ��c(H2SO4)Ϊ0.0500 mol��L��1��n(H2SO4)Ϊ0.0500 mol�� ����Zn��2H2SO4(Ũ) ��������2n(SO2)��������������n(SO2) ����Zn��H2SO4(ϡ) ��������n(H2)����������������n(H2) ���� ������ã�n(SO2)��0.300 mol��n(H2)��1.20 mol ������V(SO2)��V(H2)��0.300 mol��1.20 mol��1��4�� |

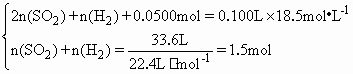
 CH3COO��+H+ ��H��0��
CH3COO��+H+ ��H��0�� CH3COO��+H+ ��H��0
CH3COO��+H+ ��H��0
