题目内容
【题目】某溶液可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 和
和![]() 某同学为了确认其成分,取部分溶液,设计并完成了如图实验:下列说法正确的是
某同学为了确认其成分,取部分溶液,设计并完成了如图实验:下列说法正确的是![]()
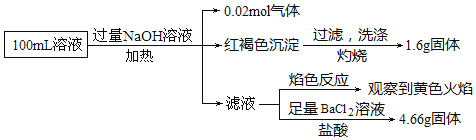
A.原溶液中![]()
B.![]() 、
、![]() 、
、![]() 一定存在,
一定存在,![]() 一定不存在
一定不存在
C.要确定原溶液中是否含有![]() ,其操作为取少量原溶液于试管中,加KSCN溶液,再加入适量氯水,溶液呈血红色,则含有
,其操作为取少量原溶液于试管中,加KSCN溶液,再加入适量氯水,溶液呈血红色,则含有![]()
D.溶液中至少有4种离子存在,其中![]() 一定存在,且
一定存在,且![]()
【答案】D
【解析】
加入过量NaOH溶液,加热,得到0.02mol气体,该气体为氨气,原溶液中一定存在0.02molNH4+;产生的红褐色沉淀为氢氧化铁,1.6g固体为三氧化二铁,氧化铁的物质的量为0.01mol,则原溶液中含有0.02mol铁元素,可能为Fe3+、Fe2+,原溶液中一定没有CO32-;滤液通入二氧化碳无现象,则原溶液中一定不存在Al3+;4.66g不溶于盐酸的固体为硫酸钡,硫酸钡的物质的量为0.02mol,原溶液中含有0.02mol硫酸根离子;颜色反应为黄色,则溶液中存在钠离子,由于加入了氢氧化钠溶液,无法判断原溶液中是否含有钠离子;根据溶液电中性判断是否存在氯离子,以此解答该题。
![]() 根据以上分析可知,原溶液中含有
根据以上分析可知,原溶液中含有![]() 铁元素,无法判断存在的是铁离子或者亚铁离子,故A错误;
铁元素,无法判断存在的是铁离子或者亚铁离子,故A错误;
B. 根据以上分析可知,原溶液中一定存在![]() 、
、![]() 、
、![]() ,只是存在
,只是存在![]() 、
、![]() 中的一种,其离子的物质的量为
中的一种,其离子的物质的量为![]() ,一定不存在
,一定不存在![]() ;由于第一步中加入了氢氧化钠溶液,引进了钠离子,无法确定原溶液中是否含有钠离子,故B错误;
;由于第一步中加入了氢氧化钠溶液,引进了钠离子,无法确定原溶液中是否含有钠离子,故B错误;
C. 检验亚铁离子时,取少量原溶液于试管中,加KSCN溶液,此时溶液现象必须是无色,然后再加入适量氯水,溶液呈血红色,则含有![]() ,否则如果加入硫氰化钾溶液后显示红色,则无法证明原溶液中是否含有亚铁离子,故C错误;
,否则如果加入硫氰化钾溶液后显示红色,则无法证明原溶液中是否含有亚铁离子,故C错误;
D. 根据以上分析,原溶液中一定存在![]() ,
,![]() ,
,![]() 、
、![]() 中的一种,当铁元素全部为亚铁离子时,阳离子所带电荷的物质的量最小,所以正电荷物质的量最少为:
中的一种,当铁元素全部为亚铁离子时,阳离子所带电荷的物质的量最小,所以正电荷物质的量最少为:![]() ,而负电荷的物质的量为:
,而负电荷的物质的量为:![]() ,根据溶液电中性可知,原溶液中一定存在
,根据溶液电中性可知,原溶液中一定存在![]() ,且
,且![]() ,故D正确;
,故D正确;
故答案选D。

【题目】下列有关实验操作、现象和结论均正确的是
选项 | 实 验 操 作 及 现 象 | 实 验 结 论 |
A | 将水蒸气通过灼热的铁粉,粉末变红褐色 | 铁与水在高温下发生反应 |
B | 向某溶液中加入几滴新制的氯水,再加入2滴KSCN溶液,溶液变为红色 | 原溶液中不一定含有 |
C | 将某气体通入酸性高锰酸钾溶液中,溶液紫色褪去 | 该气体有还原性 |
D | 用pH试纸测定NaClO溶液的酸碱性,试纸显蓝色 | NaClO水解显碱性 |
A.AB.BC.CD.D




