题目内容
20.①在氢氧化铁胶体中加入硫酸,先产生红褐色沉淀后沉淀溶解,②用半透膜把制作的氢氧化铁胶体中含有的NaCl分离出来.请从下面的选项中选出以上操作和现象涉及到胶体性质适宜的词语填入空格中(填编号):③②⑧①①渗析 ②溶解 ③聚沉 ④凝胶 ⑤布朗运动 ⑥电泳 ⑦丁达尔现象 ⑧中和 ⑨水解.
分析 在氢氧化铁胶体中加入硫酸,发生胶体的聚沉,先产生红褐色沉淀,氢氧化铁具有碱性,和硫酸发生中和反应,后沉淀溶解,胶体不能透过半透膜,用半透膜把制作的氢氧化铁胶体中含有的NaCl分离出来,为胶体的提纯,据此分析解答.
解答 解:胶体遇电解质溶液能发生聚沉,在氢氧化铁胶体中加入硫酸,发生胶体的聚沉,先产生红褐色沉淀,现象选③,氢氧化铁具有碱性,和硫酸发生中和反应,后沉淀溶解,
现象选②,性质为中和反应,选⑧,胶体不能透过半透膜,而溶液可以,将胶体和溶液用半透膜分离的方法叫渗析,所以用半透膜把制作的氢氧化铁胶体中含有的NaCl分离出来,选①,
故答案为:③②⑧①.
点评 本题考查胶体的性质,题目难度不大,注意胶体聚沉性质和氢氧化铁碱性的掌握.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
10.下列化学用语表达正确的是( )
| A. | 中子数为10的氧原子:${\;}_{10}^{18}$O | B. | 羟基的电子式: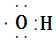 | ||
| C. | Na2S的电子式: | D. | CO2的结构式:O-C-O |
11.工业上以铬铁矿(主要成分为FeO•Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7•2H2O),其主要反应为:(1)4FeO•Cr2O3+8Na2CO3+7O2$\frac{\underline{\;高温\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2
(2)2Na2CrO4+H2SO4?Na2SO4+Na2Cr2O7+H2O 下列说法中正确的是( )
(2)2Na2CrO4+H2SO4?Na2SO4+Na2Cr2O7+H2O 下列说法中正确的是( )
| A. | 反应(1)和(2)均为氧化还原反应 | |
| B. | 反应(1)的氧化剂是O2,还原剂是FeO•Cr2O3 | |
| C. | 高温下,O2的氧化性大于Fe2O3小于Na2CrO4 | |
| D. | 生成1mol的Na2Cr2O7时共转移5mol电子 |
8.金属Ti(钛)是一种具有许多优良性能的较为昂贵的金属,钛和钛合金被认为是21世纪的重要金属材料.某化学兴趣小组用实验探究Ti、Mg、Cu的活泼性顺序.他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度的足量稀硫酸中,观察现象如下:
下列有关三种金属的说法正确的是( )
下列有关三种金属的说法正确的是( )
| 金属 | Ti | Mg | Cu |
| 金属表面现象 | 放出气泡速度缓慢 | 放出气泡速度快 | 无变化 |
| A. | 在地壳中的含量Mg>Ti,说明金属在地壳中的含量越低,活泼性越弱 | |
| B. | 反应中产生H2速李不同的原因是因为c(H+)不同 | |
| C. | 用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径 | |
| D. | 利用电解装置,Cu可以与稀硫酸反应产生H2 |
15.由已知电离常数判断,下列关于SO2与Na2CO3(aq)反应的离子方程式的书写中,不合理的是( )
| 酸 | 电离常数 |
| 碳酸 | K1=4×10-7 K2=5.6×10-11 |
| 亚硫酸 | K1=1.54×10-2 K2=1.02×10-7 |
| A. | SO2+H2O+2CO32-=2HCO3-+SO32- | B. | SO2+2HCO3-=2CO2+SO32-+H2O | ||
| C. | 2SO2+H2O+CO32-=CO2+2HSO3- | D. | SO2+H2O+CO32-=HCO3-+HSO3- |
5. 已知图一表示的是可逆反应A(g)+B(g)?C(s)+D(g)△H>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)?N2O4(g)△H<0的浓度(c)随时间t的变化情况.下列说法中正确的是( )
已知图一表示的是可逆反应A(g)+B(g)?C(s)+D(g)△H>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)?N2O4(g)△H<0的浓度(c)随时间t的变化情况.下列说法中正确的是( )
 已知图一表示的是可逆反应A(g)+B(g)?C(s)+D(g)△H>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)?N2O4(g)△H<0的浓度(c)随时间t的变化情况.下列说法中正确的是( )
已知图一表示的是可逆反应A(g)+B(g)?C(s)+D(g)△H>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)?N2O4(g)△H<0的浓度(c)随时间t的变化情况.下列说法中正确的是( )| A. | 若图一t2时改变的条件是增大压强,则反应的△H增大 | |
| B. | 图一t2时改变的条件可能是升高了温度或增大了压强 | |
| C. | 图二t1时改变的条件可能是升高了温度或增大了压强 | |
| D. | 若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将减小 |
12.下列有机物若是炔烃与氢气的加成产物,则炔烃可能的结构有( )种


| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
9.NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 1mol NaBH4与足量水反应(NaBH4+H2O→NaBO2+H2↑,未配平)时转移的电子数为8NA | |
| B. | 1 L 0.1mol•L-1NaF溶液中含有0.1NA个F- | |
| C. | 常温常压下,1mol NaHCO3与足量稀硫酸反应,生成气体的体积大于22.4L | |
| D. | 在标准状况下,22.4L氢气与22.4L氦气所含有的原子数均为2NA |
10.在配制一定物质的量浓度的NaOH溶液时,造成实验结果可能偏高的是( )
| A. | 转移时有溶液洒落在外 | B. | 定容时观察液面俯视 | ||
| C. | 有少量NaOH溶液残留在烧杯里 | D. | 容量瓶中原来有少量蒸馏水 |