题目内容
|
将足量CO2通入KOH和Ca(OH)2的混合稀溶液中,下面表示生成沉淀的物质的量(n)和通入CO2的体积(V)的关系正确的是 | |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|
答案:D
解析:
解析:
|
解析:本题属于反应的进程题.从化学原理分析,反应应分为三个阶段:第一阶段是发生反应Ca2++2OH-+CO2=CaCO3↓+H2O,若认为有下列反应同时发生:2KOH+CO2=K2CO3+H2O,由于有Ca(OH)2的存在,则反应Ca(OH)2+K2CO3=CaCO3↓+2KOH随之发生,相当于KOH没有参与反应;第二阶段是发生反应2OH-+CO2= 评注:对于图象题,要注意看清横坐标、纵坐标的意义,曲线的起点、转折点、终点的位置和含义,并分析图中曲线的变化. |

练习册系列答案
相关题目
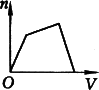
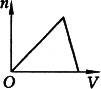
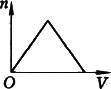
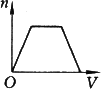
 (2012?奉贤区二模)将足量CO2通入KOH和Ca(OH)2混合溶液,生成沉淀的物质的量和通入CO2体积(V)的关系正确的是( )
(2012?奉贤区二模)将足量CO2通入KOH和Ca(OH)2混合溶液,生成沉淀的物质的量和通入CO2体积(V)的关系正确的是( )

