题目内容
| |||||||||||||||
答案:2.44;
解析:
解析:
(1) |
H++OH-=H2O,CO32-+H+=HCO3- |
(3) |
解:由CO32-+2H+=H2O+CO2↑得: n(CO2)=n(H+)=n(HCl)=(0.045L—0.025L)×1mol/L=0.020mol(1分) 设Na2CO3、Na2CO3的物质的量分别为x、y,由碳原子守恒得: x+y=0.02①(1分) 由此可知,n(NaOH)=1mol/L×0.005L=0.005mol 由NaOH+NaHCO3=Na2CO3+H2O知,与碳酸氢钠反应的NaOH为y,原混合物中:n(NaOH)=0.005+y (1分) 106g/moL×x+84mol/L×y+40g/mol×(y+0005mol)=2.5g② 解之①②得:x=y=0.01mol(1分) w(Na2CO3)=(106g/mol×0.01mol)/2.5g×100%=42.4%(1分) 答:原混合物中Na2CO3的质量分数为42.4%. |

练习册系列答案
相关题目
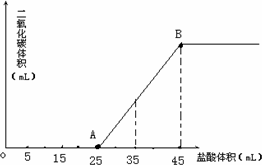

 (2009?湘潭一模)将2.5g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol?L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:
(2009?湘潭一模)将2.5g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol?L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:

