题目内容
7.将铁屑溶于过量盐酸后,再加入下列物质,会有三价铁生成的是( )| A. | 硫酸 | B. | 硫酸铜 | C. | 氯水 | D. | 氯化铜 |
分析 铁屑溶于过量盐酸后,反应生成氯化亚铁,再加氧化性物质可将亚铁离子氧化为铁离子,以此来解答.
解答 解:铁屑溶于过量盐酸后,反应生成氯化亚铁,
A.硫酸与氯化亚铁不反应,故A不选;
B.硫酸铜与氯化亚铁不反应,故B不选;
C.氯水可与氯化亚铁反应生成氯化铁,故C选;
D.氯化铜与氯化亚铁不反应,故D不选;
故选C.
点评 本题考查金属单质的性质及氧化还原反应,为高频考点,把握元素化合物知识及氯水的成分和性质为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.2007年诺贝尔化学奖得主Gerhard Ertl对金属Pt表面催化CO氧化反应的模型进行了深入研究.下列关于
${\;}_{78}^{202}$Pt的说法正确的是( )
${\;}_{78}^{202}$Pt的说法正确的是( )
| A. | ${\;}_{78}^{202}$Pt和${\;}_{78}^{198}$Pt的质子数相同,互称为同位素 | |
| B. | ${\;}_{78}^{202}$Pt和${\;}_{78}^{198}$Pt的中子数相同,互称为同位素 | |
| C. | ${\;}_{78}^{202}$Pt和${\;}_{78}^{198}$Pt是同一种核素 | |
| D. | ${\;}_{78}^{202}$Pt和${\;}_{78}^{198}$Pt的质量数不同,不能互称为同位素 |
18.某研究性学习小组设计除去锅炉水垢(CaCO3、Mg(OH)2、CaSO4)的实验,查找各物质的溶解度数据如下.
设计流程如下(所加的试剂均过量):
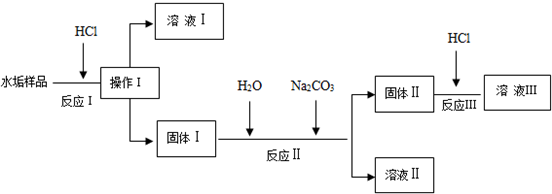
(1)操作Ⅰ的名称是过滤.
(2)溶液Ⅰ和溶液Ⅲ都含有的溶质是HCl、CaCl2.
(3)写出发生在上述过程中符合“盐+酸=另一种盐+另一种酸”特征的反应方程式CaCO3+2HCl=CaCl2+CO2↑+H2O.
写出反应Ⅱ的离子方程式CaSO4+CO32-=CaCO3+SO42-.
(4)上述过程中哪一步反应是利用了上述溶解度表设计的B.
A.反应ⅠB.反应ⅡC.反应Ⅲ
(5)溶液Ⅱ中的含氧酸根的检验方法是:取少量溶液II,先加盐酸无现象,再加氯化钡生成白色沉淀,则证明含硫酸根离子.
| 化学式 | CaSO4 | CaCO3 | Ca(OH)2 | CaCl2 |
| 溶解度/g | 0.21 微溶 | <0.01 | 0.077 | 74.5 |

(1)操作Ⅰ的名称是过滤.
(2)溶液Ⅰ和溶液Ⅲ都含有的溶质是HCl、CaCl2.
(3)写出发生在上述过程中符合“盐+酸=另一种盐+另一种酸”特征的反应方程式CaCO3+2HCl=CaCl2+CO2↑+H2O.
写出反应Ⅱ的离子方程式CaSO4+CO32-=CaCO3+SO42-.
(4)上述过程中哪一步反应是利用了上述溶解度表设计的B.
A.反应ⅠB.反应ⅡC.反应Ⅲ
(5)溶液Ⅱ中的含氧酸根的检验方法是:取少量溶液II,先加盐酸无现象,再加氯化钡生成白色沉淀,则证明含硫酸根离子.
15.下列说法错误的是( )
| A. | 1 mol 氢 | B. | 1 mol O | C. | 1 mol 二氧化碳 | D. | 1 mol水 |
12.粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,除去这些杂质的试剂可选用①Na2CO3、②NaOH、③BaCl2、④HCl,加入的先后顺序可以是( )
| A. | ①②③④ | B. | ②③①④ | C. | ②①③④ | D. | ③②①④ |
16.一定条件下,在密闭容器内,SO2氧化成SO3的热化学方程式为:2SO2(g)+O2(g)?2SO3(g);△H=-a kJ•mol-1在相同条件下,要想得到 a kJ热量,加入各物质的物质的量可能的是( )
| A. | 2 molSO2和1molO2 | B. | 2molSO2和2molO2 | ||
| C. | 3molSO2和1.5molO2 | D. | 1molSO2、0.5molO2和1molSO3 |
10.把m molC2H4跟n molH2混合在密闭容器中,在适当条件下,反应达到平衡时生成p molC2H6,若将所得平衡混和气体完全燃烧生成二氧化碳和水,需要氧气的量为( )
| A. | 3m+nmol | B. | 3m+$\frac{n}{2}$mol | C. | $\frac{3m+3p+n}{2}$mol | D. | $\frac{3m+n}{2-3p}$mol |



