��Ŀ����
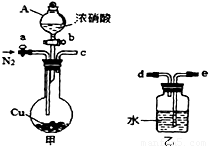
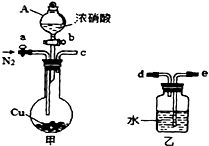 ij��ѧ����С��������ͼʵ��װ�ã��г�������ȥ����̽��ͭ��Ũ���ᷴӦ�Ƿ���NO���ɣ�
ij��ѧ����С��������ͼʵ��װ�ã��г�������ȥ����̽��ͭ��Ũ���ᷴӦ�Ƿ���NO���ɣ�
��ش��������⣺
��1������A��������______��
��2����װ�õ�cӦ������װ�õ�______���ӣ��d����e������
��3����װ���з�Ӧ�Ļ�ѧ����ʽ��______��
��4��ʵ�鲽�����£�
i������װ��ϣ����װ�õ������ԣ������Լ���������a��ͨ��N2һ��ʱ��ر�����a��
ii������b���μ���xmol?L-1Ũ����V mL����ַ�Ӧ����ȴ����������ʣ�࣮
iii��NaOH��Һ�ζ���װ������Һ�������ʵ����ʵ���Ϊn mol��
�ٲ���iͨ��N2��Ŀ����______
��Ϊ��ȷ�ⶨ��װ���в���NO2�������ڲ���ii��iii֮��Ӧ����IJ����ǣ�______��
�۵�xV��l0-3______3n�����������=������������֤��ͭ��Ũ���ᷴӦʱ��NO���ɣ�
�ܸ�ʵ������д���һ�����Ե�ȱ����______��
�⣺��1������A�������Ƿ�Һ©�����ʴ�Ϊ����Һ©����
��2����װ�õ�cӦ������װ�õ�e����ʹ���屻ˮ���գ��ʴ�Ϊ��e��
��3������������ˮ��Ӧ����������NO����Ӧ����ʽΪ��3NO2+H2O=2HNO3+NO���ʴ�Ϊ��3NO2+H2O=2HNO3+NO��
��4��������װ���вд�Ŀ�����������NO����ʵ��������ţ����Եμ�ŨHNO3֮ǰ��Ҫͨ��һ��ʱ�䵪������װ���еĿ�����
�ʴ�Ϊ���Ͼ�װ���еĿ�����
��Ϊ��֤���ɵ�������ȫ��ˮ���գ�Ӧ��a���ر�b��ͨ��N2һ��ʱ�䣬
�ʴ�Ϊ����a���ر�b��ͨ��N2һ��ʱ�䣻
�۸���Cu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O��3NO2+H2O=2HNO3+NO�ɵù�ϵʽ9HNO3��Ũ����4.5NO2��3HNO3����NaOH�ζ�����xV��l0-3=3n����˵��û������NO����xV��l0-3��3n�����˵������NO���ʴ�Ϊ������
�ܵ�������Կ�������Ⱦ������ֱ���ŷŵ������У�Ӧ��β������װ�ã��ʴ�Ϊ��ȱ��β������װ�ã�
������Cu��ŨHNO3��Ӧ����Cu��NO3��2��NO2��H2O����Ӧ����ʽΪCu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O��
������NO������3Cu+8HNO3=3Cu��NO3��2+2NO��+4H2O������������ˮ��Ӧ����������NO����Ӧ����ʽΪ��3NO2+H2O=2HNO3+NO������װ���вд�Ŀ�����������NO����ʵ��������ţ�ʵ����Ҫͨ�뵪��������֤����ȫ�������գ�����Cu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O��3NO2+H2O=2HNO3+NO�ɵù�ϵʽ9HNO3��Ũ����4.5NO2��3HNO3����NaOH�ζ�����xV��l0-3=3n����˵��û������NO����xV��l0-3��3n�����˵������NO���Դ˽����⣮
������������������ͭ�ķ�ӦΪ���壬�ۺϿ���ѧ��ʵ����ƺ�̽��������ע��������ʵ������Լ����ʵ������Ļ�����������Ŀ�Ѷ��еȣ��״���Ϊ��4����ע�����ù�ϵʽ���
��2����װ�õ�cӦ������װ�õ�e����ʹ���屻ˮ���գ��ʴ�Ϊ��e��
��3������������ˮ��Ӧ����������NO����Ӧ����ʽΪ��3NO2+H2O=2HNO3+NO���ʴ�Ϊ��3NO2+H2O=2HNO3+NO��
��4��������װ���вд�Ŀ�����������NO����ʵ��������ţ����Եμ�ŨHNO3֮ǰ��Ҫͨ��һ��ʱ�䵪������װ���еĿ�����
�ʴ�Ϊ���Ͼ�װ���еĿ�����
��Ϊ��֤���ɵ�������ȫ��ˮ���գ�Ӧ��a���ر�b��ͨ��N2һ��ʱ�䣬
�ʴ�Ϊ����a���ر�b��ͨ��N2һ��ʱ�䣻
�۸���Cu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O��3NO2+H2O=2HNO3+NO�ɵù�ϵʽ9HNO3��Ũ����4.5NO2��3HNO3����NaOH�ζ�����xV��l0-3=3n����˵��û������NO����xV��l0-3��3n�����˵������NO���ʴ�Ϊ������
�ܵ�������Կ�������Ⱦ������ֱ���ŷŵ������У�Ӧ��β������װ�ã��ʴ�Ϊ��ȱ��β������װ�ã�
������Cu��ŨHNO3��Ӧ����Cu��NO3��2��NO2��H2O����Ӧ����ʽΪCu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O��
������NO������3Cu+8HNO3=3Cu��NO3��2+2NO��+4H2O������������ˮ��Ӧ����������NO����Ӧ����ʽΪ��3NO2+H2O=2HNO3+NO������װ���вд�Ŀ�����������NO����ʵ��������ţ�ʵ����Ҫͨ�뵪��������֤����ȫ�������գ�����Cu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O��3NO2+H2O=2HNO3+NO�ɵù�ϵʽ9HNO3��Ũ����4.5NO2��3HNO3����NaOH�ζ�����xV��l0-3=3n����˵��û������NO����xV��l0-3��3n�����˵������NO���Դ˽����⣮
������������������ͭ�ķ�ӦΪ���壬�ۺϿ���ѧ��ʵ����ƺ�̽��������ע��������ʵ������Լ����ʵ������Ļ�����������Ŀ�Ѷ��еȣ��״���Ϊ��4����ע�����ù�ϵʽ���

��ϰ��ϵ�д�
 ����ʦ��Сһ����ʦ������ҵϵ�д�
����ʦ��Сһ����ʦ������ҵϵ�д� ���100�ֵ�Ԫ�Ż�������ϵ�д�
���100�ֵ�Ԫ�Ż�������ϵ�д�
�����Ŀ
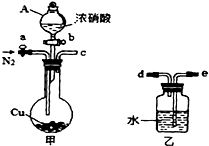 ��2012?����ģ�⣩ij��ѧ����С��������ͼʵ��װ�ã��г�������ȥ����̽��ͭ��Ũ���ᷴӦ�Ƿ���NO���ɣ�
��2012?����ģ�⣩ij��ѧ����С��������ͼʵ��װ�ã��г�������ȥ����̽��ͭ��Ũ���ᷴӦ�Ƿ���NO���ɣ�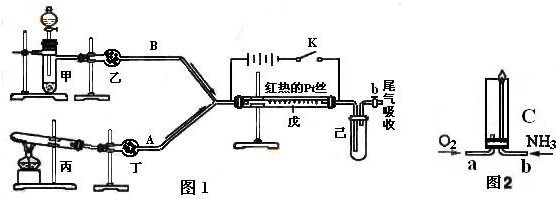
 ij����С��������ͼװ�ý������ʵ�飬��ش��������⣮
ij����С��������ͼװ�ý������ʵ�飬��ش��������⣮