题目内容
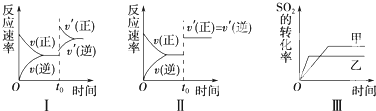
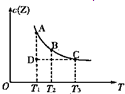 在容积不变的密闭容器中投入一定量的X 和Y有反应:X(g)+Y(g)?Z(g),若Z(g)的物质的量浓度c(Z)与温度T的关系如右图所示(曲线上的任意一点都表示平衡状态).则下列说法不正确的是( )
在容积不变的密闭容器中投入一定量的X 和Y有反应:X(g)+Y(g)?Z(g),若Z(g)的物质的量浓度c(Z)与温度T的关系如右图所示(曲线上的任意一点都表示平衡状态).则下列说法不正确的是( )分析:A、由图可知,温度越高平衡时c(Z)越小,说明升高温度平衡向逆反应移动,A点与B点相比,A点的c(X)大;
B、由图可知,A点在曲线上属于平衡状态据此分析速率;
C、在反应进行到D点时,没有到达平衡状态,所以V正>V逆;
D、温度越高平衡时c(Z)越小,说明升高温度平衡向逆反应移动.
B、由图可知,A点在曲线上属于平衡状态据此分析速率;
C、在反应进行到D点时,没有到达平衡状态,所以V正>V逆;
D、温度越高平衡时c(Z)越小,说明升高温度平衡向逆反应移动.
解答:解:A、由图可知,温度越高平衡时c(Z)越小,说明升高温度平衡向逆反应移动,A点与B点相比,A点的c(X)大,故A错误;
B、由图可知,A点在曲线上属于平衡状态,所以A点v正=v逆;故B正确;
C、在反应进行到D点时,没有到达平衡状态,要达到平衡c(Z)的浓度要增大,即向正反应方向移动,所以V正>V逆;故C正确;
D、温度越高平衡时c(Z)越小,说明升高温度平衡向逆反应移动,所以正反应为放热反应,故D正确;
故选A.
B、由图可知,A点在曲线上属于平衡状态,所以A点v正=v逆;故B正确;
C、在反应进行到D点时,没有到达平衡状态,要达到平衡c(Z)的浓度要增大,即向正反应方向移动,所以V正>V逆;故C正确;
D、温度越高平衡时c(Z)越小,说明升高温度平衡向逆反应移动,所以正反应为放热反应,故D正确;
故选A.
点评:本题以化学平衡图象为载体,考查温度对平衡移动的影响,难度中等,注意曲线的各点都处于平衡状态.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
在容积不变的密闭容器中进行反应:2SO2( g )+O2( g)?2SO3(g );△H<O.如图表示当其它条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )
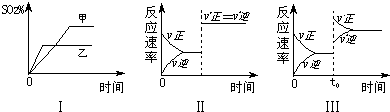

| A、图Ⅰ表示温度对化学平衡的影响,且甲的温度较高 | B、图Ⅱ表示t0时刻使用催化剂对反应速率的影响 | C、图Ⅱ表示t0时刻通入氦气对反应速率的影响 | D、图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响 |