题目内容
13.下列说法正确的是( )| A. | 元素的价电子数和族序数相等 | B. | 酸性:HClO4>H2SO4>H3PO4 | ||
| C. | IA、IIB族的元素属于S区元素 | D. | [Cu(NH3)4]2+离子中的配位键数为3. |
分析 A.主族元素的价电子数等于其所在族的族序数,零族元素、一些副族元素等价电子数不一定等于其所在族的族序数;
B.同周期自左而右非金属性增强,非金属性越强,最高价含氧酸的酸性越强;
C.IIB族的元素属于d区元素;
D.Cu2+离子与4个NH3分子形成配位键.
解答 解:A.主族元素的价电子数等于其所在族的族序数,零族元素、一些副族元素、第VIII族元素的价电子数不等于其所在族的族序数,故A错误;
B.同周期自左而右非金属性增强,非金属性越强,最高价含氧酸的酸性越强,故酸性:HClO4>H2SO4>H3PO4,故B正确;
C.IA族的元素属于s区元素,但IIB族的元素属于d区元素,故C错误;
D.Cu2+离子与4个NH3分子形成4个配位键,故D错误,
故选B.
点评 本题考查元素周期表、元素周期律、结构与位置关系、配位键,比较基础,侧重对基础知识的巩固.

练习册系列答案
相关题目
4.关于化学键的下列叙述正确的是( )
| A. | 离子化合物中只含离子键 | B. | 共价化合物中不含离子键 | ||
| C. | 离子化合物中不可能含共价键 | D. | 共价化合物中可能含离子键 |
1.下列变化中发生取代反应的是( )
| A. | 苯与溴水混合,水层褪色 | |
| B. | 乙烯使溴的四氯化碳溶液褪色 | |
| C. | 乙烷与氯气反应制氯乙烷 | |
| D. | 苯和氯气在一定条件下生成六氯环已烷 |
8.下列事实与电化学原理无关的是( )
| A. | 金属铝在空气中不易被腐蚀 | |
| B. | 铁制器件在潮湿空气中生锈 | |
| C. | 镀锌铁片比镀锡铁片更耐腐蚀 | |
| D. | 远洋海轮的外壳连接锌块可保护轮船不受腐蚀 |
18.能够测定分子结构和化学键的方法是( )
| A. | 质谱 | B. | 红外光谱 | C. | 紫外光谱 | D. | 核磁共振氢谱 |
2.下列说法错误的是( )
| A. | ⅠA族金属元素是同周期中金属性最强的元素 | |
| B. | ⅤⅡA族元素的阴离子还原性越强,其最高价氧化物对应的水化物的酸性越强 | |
| C. | 主族元素气态氢化物越稳定,其非金属性越强 | |
| D. | 同周期主族元素原子序数越大,其非金属越强 |
3. 已知某碱性硼化矾(VB2)-空气电池工作时发生反应为:11O2+4VB2═2V2O5+4B2O3.以该电池作为电源,使用惰性电极电解硫酸铜溶液,实验装置如图所示.当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是( )
已知某碱性硼化矾(VB2)-空气电池工作时发生反应为:11O2+4VB2═2V2O5+4B2O3.以该电池作为电源,使用惰性电极电解硫酸铜溶液,实验装置如图所示.当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是( )
 已知某碱性硼化矾(VB2)-空气电池工作时发生反应为:11O2+4VB2═2V2O5+4B2O3.以该电池作为电源,使用惰性电极电解硫酸铜溶液,实验装置如图所示.当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是( )
已知某碱性硼化矾(VB2)-空气电池工作时发生反应为:11O2+4VB2═2V2O5+4B2O3.以该电池作为电源,使用惰性电极电解硫酸铜溶液,实验装置如图所示.当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是( )| A. | VB2电极发生的电极反应为:2VB2+11H2O-22e-═V2O5+2B2O3+22H+ | |
| B. | 若B装置内的液体体积为400mL,则CuSO4溶液的物质的量浓度为0.025mol/L | |
| C. | 电解过程中,b电极表面先有红色物质析出,然后有气泡产生 | |
| D. | 外电路中电子由a电极流向b电极 |
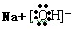 ,含有化学键的类型离子键、极性键;
,含有化学键的类型离子键、极性键;  草酸(HOOC-COOH)是一种重要的化工原料和化工产品.利用石油化工产品中的烷烃可以生成草酸,生产流程如下:已知上述框图中有机物B的相对分子质量比有机物A的相对分子质量大79.请回答下列问题:
草酸(HOOC-COOH)是一种重要的化工原料和化工产品.利用石油化工产品中的烷烃可以生成草酸,生产流程如下:已知上述框图中有机物B的相对分子质量比有机物A的相对分子质量大79.请回答下列问题: