题目内容
|
按F2、Cl2、Br2、I2的顺序,下列变化规律中不正确的是 ①单质颜色逐渐加深 ②密度逐渐增大 ③熔点与沸点逐渐升高 ④X2的氧化性增强 ⑤HX稳定性减弱 ⑥X-还原性减弱 ⑦与H2反应逐渐困难 ⑧与水反应逐渐困难 | |
A. |
①③ |
B. |
②⑤ |
C. |
④⑥ |
D. |
⑦⑧ |
答案:C
解析:
解析:
|
卤素单质性质变化是有规律的,其物理性质变化规律如下: F2 Cl2 Br2 I2 淡黄绿色 黄绿色 红棕色 紫黑色 气体 气体 液体 固体 颜色 状态 密度 熔沸点 水中溶解度 由于从F→I,其原子的电子层数增加,原子半径增大,得电子能力减弱,失电子能力增强,且由于它们最外层电子数相同,故其化学性质存在相似性和递变性. 相似性表现在卤素单质均有很强或较强的非金属性,以氧化性为主要性质,可以与金属、某些非金属(如H2)、水和碱溶液反应.其气态氢化物均易溶于水形成氢卤酸.HX在空气中均可形成白雾.卤素X-最外层均为8电子稳定结构,只有还原性而无氧化性. 其递变规律表示如下: 单质的氧化性 卤素离子(X-)还原性 与H2反应 气态氢化物(HX)稳定性 气态氢化物的还原性 氢卤酸的酸性 由以上性质变化情况可知④⑥是错误的. |

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
卤素单质及化合物在许多性质上都存在着递变规律.下列有关说法正确的是( )
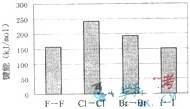
| A、卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深 | B、卤化氢的键长按H-F、H-C1、H-Br、H-I的顺序依次减小 | C、卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱 | D、卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易 |
 (2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.
(2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.
