题目内容
短周期主族元素A、B、C、D,原子序数依次增大。A、B、C三种元素原子的最外层电子数之和为15,A、C的原子序数的差为8,A原子最外层电子数等于B原子最外层电子数的2倍。下列叙述正确的是
A.原子半径:A<D<C<B
B.非金属性:C>D
C.氢化物的热稳定性:C>A
D.单质B常温下能溶于浓硝酸但不能溶于氢氧化钠溶液
【答案】
A
【解析】
试题分析:A、C的原子序数的差为8,则在短周期元素中,二者一定是同一主族的元素。A原子最外层电子数等于B原子最外层电子数的2倍,又因为A、B、C三种元素原子的最外层电子数之和为15,所以B元素最外层电子数是15÷5=3,因此根据A、B、C、D原子序数依次增大可知,A是氧元素,B是铝元素,C是S元素,则D是氯元素,A正确;B不正确,非金属性:C<D;氢化物的稳定性是C<A,C不正确;D不正确,铝在常温下和浓硝酸发生钝化,但可以溶解在氢氧化钠溶液中,答案选A。
考点:考查元素周期表的结构和元素周期律的应用
点评:该题是中等难度的试题,也是高考中的常见题型。试题注重基础,侧重能力的培养。该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目
短周期主族元素A、B、C、D的原子序数依次增大.A、C原子序数相差8,A、B、C三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半.下列叙述正确的是( )
| A、原子半径:A<D<C<B | B、B、C、D分别与A形成的化合物一定含有相同的化学键 | C、最高价氧化物对应水化物的酸性:D<C | D、常温下,单质B能大量溶于浓硝酸中 |
短周期主族元素A、B、C的原子序数依次递增,A与C同主族,B原子的最外层电子数等于A原子的次外层电子数,它们原子的最外层电子数之和为10,则下列叙述正确的是( )
| A、原于半径A<B<C | B、A的气态氢化物稳定性大于C的气态氢化物稳定性 | C、A、C两元素最高价氧化物均可与水化合得到对应的酸 | D、高温时,A单质可以从C的氧化物中置换得到C单质 |
短周期主族元素A、B、C、D、E的原子序数依次增大,其中A与C同主族,A与其它元素不在同一周期,B与D同主族,常温下D的单质为淡黄色固体.下列推断中正确的是( )
| A、原子半径由小到大的顺序:r(C)<r(D)<r(E) | B、元素D、E分别与A形成的化合物的热稳定性:E>D | C、元素D的最高价氧化物对应水化物的酸性比E的强 | D、元素B分别与A、C形成的化合物中化学键的类型完全相同 |
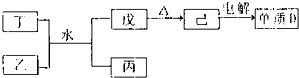
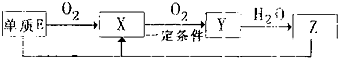
 短周期主族元素A、B、C、D、E的原子序数依次增大,它们原子核外的电子层数之和为10;B元素的化合物种类繁多,数目庞大.C、D两种元素形成的单质是空气中含量最多的物质;D、E两元素可以生成两种不同的离子化合物.
短周期主族元素A、B、C、D、E的原子序数依次增大,它们原子核外的电子层数之和为10;B元素的化合物种类繁多,数目庞大.C、D两种元素形成的单质是空气中含量最多的物质;D、E两元素可以生成两种不同的离子化合物. NH3?H2O+H+
NH3?H2O+H+ 2NO2
2NO2