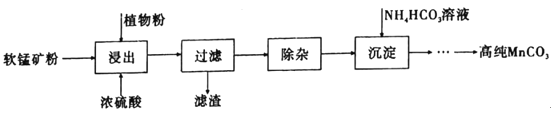
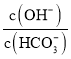��Ŀ����
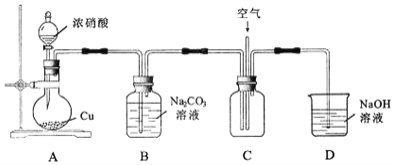
����Ŀ��ijУ��ѧ�����о�С��Ϊ��֤Ũ���������Zn��Ӧ�����������к�SO2��H2������������ʵ����
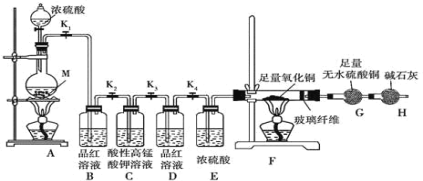
��1����װ��ҩƷǰ����ͬѧ����װ��_____��
��2����д�±��е�ʵ������_____��
װ�� | B | F | G |
ʵ������ |
��3��װ��C��������_____��д��װ��C�з�����Ӧ�����ӷ���ʽ_____��
��4��װ��D��������_____��
��5��SO2�Ǵ�����Ⱦ��֮һ��Ҳ��ij��ҵ�����е���Ҫβ��֮һ��ijУ��ȤС�����������з����ⶨ�˹�ҵβ���е�SO2�ĺ�����
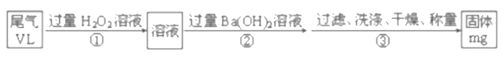
ͨ����β�����ΪVL���ѻ���ɱ�״����ʱ����β����SO2���������������Ϊ_____���ú���V��m�Ĵ���ʽ��ʾ����
���𰸡�������
װ�� | B | F | G |
ʵ������ | Ʒ����ɫ | ��ɫ������ | ��ɫ������� |
��ȥ����δ��Ӧ���SO2 5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+ ����SO2�Ƿ��ѳ��� ![]()
��������
��ͼ����Ϣ��֪��AΪŨ������п��Ӧ��װ�ã�B���ڼ����������C�������ն�������D���ڼ�����������ѳ�����E���ڸ���������F��C���ڼ���������H��Ϊ�˷�ֹ�����е�ˮ��������ʵ�飻�ⶨ��ҵβ���е�SO2�ĺ�����ʵ���У���ͨ��˫��ˮ���ն�������Ȼ������Һ������������Ӧ�������ᱵ���������ͨ�����ᱵ�������ⶨSO2�ĺ������ݴ˽��
��1����װ��ҩƷǰ����ͬѧ����װ�õ������ԡ�
��2��Ũ������п��Ӧ�����ɶ���������������Ư���ԣ���ʹƷ����Һ��ɫ���������Ũ�ȱ�ý�Сʱ��������п��Ӧ�����������������Խ���ɫ������ͭ��ԭΪ��ɫ��ͭ��ͬʱ���ɵ�ˮ��������ʹ��ɫ������ͭ��������ʵ���������Ϊ�±���
װ�� | B | F | G |
ʵ������ | Ʒ����ɫ | ��ɫ������ | ��ɫ������� |
��3��װ��C�������dz�ȥ����δ��Ӧ���SO2����ֹ����������ļ��顣װ��C�У������������Ը��������Һ����Ϊ���ᣬ������ر���ԭΪ�����̣��ʸ÷�Ӧ�����ӷ���ʽΪ5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+��
��4��װ��D�������Ǽ���SO2�Ƿ��ѳ�����ֻ�г���SO2���ܱ�֤����ʵ�����Ч�ԡ�
��5����ͼ�����ݿ�֪�����õ����ᱵ����������Ϊmg������SԪ���غ��֪��n(SO2)=n(BaSO4)= ![]() mol�����ڱ�״���£�V(SO2)=
mol�����ڱ�״���£�V(SO2)= ![]() L������ͨ����β�����ΪVL���ѻ���ɱ�״���������β����SO2���������������Ϊ
L������ͨ����β�����ΪVL���ѻ���ɱ�״���������β����SO2���������������Ϊ![]() ��
��

����Ŀ�������£���![]()
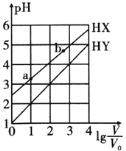
![]() ��������ˮ���100mL��Һ������Һ�м����������ʣ��йؽ�����ȷ����( )
��������ˮ���100mL��Һ������Һ�м����������ʣ��йؽ�����ȷ����( )
��������� | ���� | |
A |
| ��Ӧ������ |
B |
| ��Һ�� |
C |
| ��ˮ������� |
D |
| ��Ӧ��ȫ����ҺpH��С�� |
A.AB.BC.CD.D
����Ŀ�����ڻ������������⼰ȼú��������������������;�dz��㷺��
��1������[CO(NH2)2]������泥�NH4CNO����Ϊ___________����ѡ���ͬһ����������ͬϵ��������ͬ���칹���������������_______�����ѡ�����������������������
��2��Һ����һ��������ϣ���֪���Ͽ�1mol���ۼ����յ������������
���ۼ� | H��H | N��H | N��N |
kJ��mol��1 | 436 | 390.8 | 946 |
��ϳɰ���Ӧ��N2(g) + 3H2 (g)= 2NH3(g) ������2mol�����ų� _________kJ��������1molN2��3molH2��һ�������·�Ӧ���ﵽƽ��ʱ�ų�36.32kJ���������ʱNH3��ռ���������Ϊ______ ����ͼװ��ֱͨ���磬Һ���ɵ���ͷ��������ù���������ת����ʽΪ�ɵ���ת��Ϊ_____�ܡ�

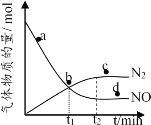
��3����������Ϊ���������ں��º����ܱ������г���һ������NO��NH3����һ�������·�����Ӧ��6NO(g) + 4NH3(g) ![]() 5N2(g) +6H2O(g)��
5N2(g) +6H2O(g)��
����˵���÷�Ӧ�Ѵﵽƽ��״̬�ı�־��_______��������ѡ��
a����Ӧ����4v ( NH3) =5v ( N2)
b��������ѹǿ������ʱ��������仯
c��������N2�����ʵ�������������ʱ��������仯
d��������n(NO)��n(NH3)��n(N2)��n(H2O) = 6��4��5��6
��ij��ʵ���в��������NO��N2�����ʵ�����ʱ��仯��ͼ��ʾ��ͼ��v (��)��v (��)��ȵĵ�Ϊ_________��ѡ����ĸ����