��Ŀ����
����Ŀ����ԴΣ���ǵ�ǰȫ���Ե����⣬����Դ��������Ӧ����ԴΣ������Ҫ�ٴ롣
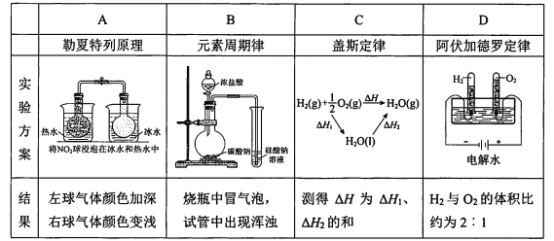
��1������������������Դ����Դ����������___(�����)��
a��������չũ���������������Ľո�ת��Ϊ����Ч����Դ
b����������ú��ʯ�ͺ���Ȼ������������������������Դ����
c������̫���ܡ�ˮ�ܡ����ܡ������ܵ�����Դ������ʹ��ú��ʯ�͵Ȼ�ʯȼ��
d��������Դ���ģ�������Դ���ظ�ʹ�á���Դ��ѭ������
��2�����ʯ��ʯī��Ϊ̼��ͬ�������壬��������������ʱȼ������һ����̼����������ʱȼ�����ɶ�����̼����Ӧ�зų���������ͼ��ʾ��
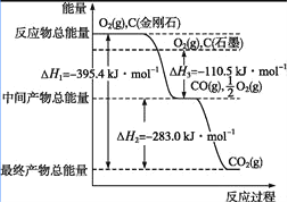
����ͨ��״���£����ʯ��ʯī��___(�������ʯ������ʯī��)���ȶ���ʯī��ȼ����Ϊ___��
��12 gʯī��һ����������ȼ�գ���������36 g���ù��̷ų�������Ϊ___��
��3����֪��N2��O2�����л�ѧ���ļ��ֱܷ���946 kJ��mol1��497 kJ��mol1��
N2(g)+O2(g)=2NO(g)��H=+180.0 kJ��mol1��
NO�����л�ѧ���ļ���Ϊ___ kJ��mol1��
���𰸡�acd ʯī 393.5kJ/mol 252 kJ 631.5
��������
��1��a��������չũ���������������Ľո�ת��Ϊ����Ч����Դ���ɼ��ٻ�ʯ��Դʹ�ã�a�������⣻
b����������ú��ʯ�ͺ���Ȼ��������������������������Դ�����ܼ��ٻ�ʯȼ�ϵ�ʹ�ã�b���������⣻
c������̫���ܡ�ˮ�ܡ����ܡ������ܵ�����Դ������ʹ��ú��ʯ�͵Ȼ�ʯȼ�ϣ���������Դ��������c�������⣻
d��������Դ���ģ�ע����Դ���ظ�ʹ�á���Դ��ѭ���������ܼ��ٻ�ʯȼ�ϵ���Դʹ�ã�d�������⣻
��ѡacd��
��2������ͼ��֪�����ʯ��������ʯī������Խ��Խ�ȶ�������˵��ʯī�ȶ���ͼ��1molʯī��ȫȼ������1mol������̼�ų�������Ϊ393.5kJ����ʯī��ȼ����Ϊ��H=-393.5kJ/mol��
��12gʯī���ʵ���Ϊ1mol����һ����������ȼ�գ�����Ԫ���غ㣬��ֻ���ɶ�����̼����Ϊ44g����ֻ����һ����̼����Ϊ28g����Ŀ����������36g��28g<36g<44g���ж����ɵ�����Ϊһ����̼�Ͷ�����̼�Ļ�����һ����̼���ʵ���Ϊx���������̼���ʵ���Ϊ(1-x)mol��28x+44(1-x)=36g�����x=0.5mol����һ����̼�Ͷ�����̼�����ʵ�����Ϊ0.5mol�����ͼ���֪��
C(ʯī��s)+O2(g)=CO2(g)��H=-393.5 kJ/mol��
C(ʯī��s)+![]() O2(g)=CO(g)��H=-110.5kJ/mol��
O2(g)=CO(g)��H=-110.5kJ/mol��
�������ɶ�����̼��һ����̼�������ų�����Ϊ��393.5kJ/mol��0.5mo1+110.5kJ/mol��0.5mo1=252kJ��
��3������N2��O2�����л�ѧ���ļ��ֱܷ���946 kJ/mol��497 kJ/mol�Լ���ӦN2(g)+O2(g)=2NO(g)��H=+180 kJ/mol����NO�����л�ѧ���ļ���Ϊa�����У�946 kJ/mol+497 kJ/mol-2a=180 kJ/mol����ã�a=631.5 kJ/mol��