题目内容
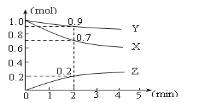
【题目】某温度时,在2L容器中三种物质的物质的量随时间的变化曲线如下图所示。由图中数据分析,该反应的化学方程式和反应开始至2min末Z的平均反应速率为( )
A.3X + Y ![]() 2Z;0.05mol·L-1·min-1B.2X + Y
2Z;0.05mol·L-1·min-1B.2X + Y![]() 2Z;0.1mol·L-1·min-1
2Z;0.1mol·L-1·min-1
C.X + 2Y =Z;0.1mol·L-1·min-1D.X + 3Y =2Z;0.05mol·L-1·min-1
【答案】A
【解析】
由图象可知,在0~2min时间段内,X、Y的物质的量分别减少0.3 mol、0.1 mol,Z的物质的量增加0.2 mol,说明X、Y是该反应的反应物,Z是该反应的产物,速率之比和各物质前面的系数成正比,由于容器的体积相同,所用时间相同,所以X、Y、Z前面的化学计量数之比等于各物质的变化量之比,即3∶1∶2,所以该反应的化学方程式为3X + Y ![]() 2Z;根据v=c/t可知,反应开始至2min末Z的平均反应速率=[0.2mol/2L]÷2min=0.05mol·L-1·min-1;故A正确;
2Z;根据v=c/t可知,反应开始至2min末Z的平均反应速率=[0.2mol/2L]÷2min=0.05mol·L-1·min-1;故A正确;
答案选A。

练习册系列答案
相关题目