题目内容
(8分)(1)在配合物Fe(SCN)2+中,提供空轨道接受孤对电子的微粒是________ _______,画出配合物离子 [Cu(NH3)4]2+中的配位键__________ __________ 。
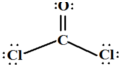
(2)根据价层电子对互斥理论模型(VSEPR模型),H3O+的分子立体结构为:__________ ________________,BCl3的立体结构为:_______ _________________。
(3)按要求写出由第二周期元素为中心原子,通过sp3杂化形成中性分子的化学式:
正四面体分子_______,三角锥形分子________,V形分子_________。(各写一种)
 (共8分) (1)Fe3+ (3分)
(共8分) (1)Fe3+ (3分)
(2)三角锥形、正三角形 (2分)
(3)CH4或CF4,NH3或NF3,H2O (3分)

练习册系列答案
相关题目
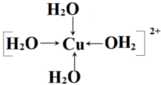
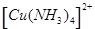 中的配位键 。
中的配位键 。 中的配位键 。
中的配位键 。