题目内容
17.下列物质,属于共价化合物的是( )| A. | I2 | B. | NH4Cl | C. | CaCl2 | D. | H2SO4 |
分析 含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,只含共价键的化合物是共价化合物,共价化合物中一定不含离子键,据此分析解答.
解答 解:A.碘分子中碘原子之间只存在共价键,但为单质,故A错误;
B.氯化铵中铵根离子和氯离子之间存在离子键、N-H原子之间存在共价键,为离子化合物,故B错误;
C.氯化钙中钙离子和氯离子之间只存在离子键,为离子化合物存,故C错误;
D.硫酸中硫氧键、硫氢键为共价键,酸为共价化合物,故D正确;
故选D.
点评 本题考查离子化合物和共价键化合物判断,为高频考点,明确物质构成微粒及微粒之间作用力是解本题关键,不能根据是否含有金属元素判断离子键,如氯化铝中只含共价键,为易错点.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
7.把元素周期表中第16号元素和第6号元素的原子相比较,下列数据中前者是后者的4倍的是( )
| A. | 电子数 | B. | 最外层电子数 | C. | 中子数 | D. | 次外层电子数 |
8.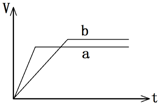 某同学在试管中用一定量的铁片与足量的稀硫酸反应,得到产生氢气的体积随时间变化的图象(b).若铁的用量不变,改变一个反应条件,得到图象(a).则改变的条件可能是( )
某同学在试管中用一定量的铁片与足量的稀硫酸反应,得到产生氢气的体积随时间变化的图象(b).若铁的用量不变,改变一个反应条件,得到图象(a).则改变的条件可能是( )
 某同学在试管中用一定量的铁片与足量的稀硫酸反应,得到产生氢气的体积随时间变化的图象(b).若铁的用量不变,改变一个反应条件,得到图象(a).则改变的条件可能是( )
某同学在试管中用一定量的铁片与足量的稀硫酸反应,得到产生氢气的体积随时间变化的图象(b).若铁的用量不变,改变一个反应条件,得到图象(a).则改变的条件可能是( )| A. | 向试管中滴加少许硫酸铜溶液 | B. | 在反应过程中对试管加热 | ||
| C. | 用铁粉代替铁片 | D. | 用98%的浓硫酸代替稀硫酸 |
5.下列有关物质性质或用途的说法不正确的是( )
| A. | 乙醇能够使蛋白质变性,75%(体积分数)的乙醇溶液可用于医疗消毒 | |
| B. | 乙二醇的水溶液凝固点很低,可用作汽车发动机的抗冻剂 | |
| C. | 光照时乙烷与氯气能发生取代反应,工业上常用该反应生产氯乙烷 | |
| D. | 乙酸( CH3COOH)与硬脂酸(C17H35COOH)互为同系物 |
12.可逆反应2NO 2?2NO+O 2在恒容密闭容器中反应,可以作为达到平衡状态的标志是( )
| A. | 单位时间内生成n mo1 O2的同时生成2n mol NO2 | |
| B. | 单位时间内生成n mol O2的同时生成2n mol NO | |
| C. | 混合气体的颜色不再改变 | |
| D. | 混合气体的密度不再改变的状态 |
2.下列叙述不能判断某化学平衡一定发生移动的是( )
| A. | 反应体系的温度改变 | |
| B. | 反应混合物中各组分的百分含量改变 | |
| C. | 正、逆反应速率改变 | |
| D. | 反应物的物质的量改变 |
9.X、Y、Z、W、R是短周期中的五种元素,其原子序数依次增大,X、W最外层电子数相等,X为地壳中含量最多的元素,Y是短周期中金属性最强的元素,Z单质是生活应用广泛的常见金属单质,下列说法不正确的是( )
| A. | 原子半径:Y>X | B. | 最高价氧化物的水化物的酸性:R>W | ||
| C. | 气态氢化物的稳定性:X>W | D. | 单质与水(或酸)反应的剧烈程度:Z>Y |
6.下列化学用语正确的是( )
| A. | CH4的比例模型: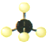 | B. | 乙醇的结构简式C2H6O | ||
| C. | 乙炔分子式:HC≡CH | D. | 丙酸的键线式: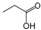 |
7.现有部分短周期元素的性质或原子结构如表:
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是146C,在周期表中的位置是第二周期 IVA族.
(2)元素Y与氢元素形成一种离子YH4+,写出该离子与Z离子形成化合物的电子式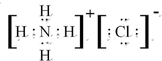 .
.
(3)写出元素X、T形成的化合物XT2的电子式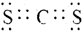 .
.
(4)元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b、d、e(填序号)
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
d.与铁加热,Z生成三价铁,T生成二价铁
e.T原子与Z原子电子层数相同,Z原子半径小于T原子
(5)T的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为SO2+Cl2+2H2O=2HCl+H2SO4
(6)分别用电子式表示Z与镁元素、Y与氮元素形成化合物的过程: ,
,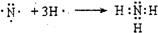 .
.
| 元素编号 | 元素性质或原子结构 |
| T | 最外层电子数比内层电子总数少4 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 与氢形成的气态化合物在标准状况下的密度为0.76g•L-1 |
| Z | 元素最高正价与负价的绝对值之差是6 |
(2)元素Y与氢元素形成一种离子YH4+,写出该离子与Z离子形成化合物的电子式
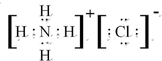 .
.(3)写出元素X、T形成的化合物XT2的电子式
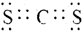 .
.(4)元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b、d、e(填序号)
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
d.与铁加热,Z生成三价铁,T生成二价铁
e.T原子与Z原子电子层数相同,Z原子半径小于T原子
(5)T的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为SO2+Cl2+2H2O=2HCl+H2SO4
(6)分别用电子式表示Z与镁元素、Y与氮元素形成化合物的过程:
 ,
,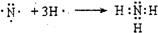 .
.