题目内容
电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为:2PbSO4+2H2O
Pb+PbO2+2H2SO4则下列说法正确的是( )
| 充电 |
| 放电 |
| A、放电时,该电池的正极材料是硫酸铅 |
| B、充电时,阳极反应是:PbSO4-2e-+2H2O=PbO2+SO42-+4H+ |
| C、充电时,电池中硫酸的浓度不断减小 |
| D、放电时,正极反应是:Pb-2e-+SO42-=PbSO4 |
分析:由铅蓄电池的总反应:2PbSO4+2H2O
Pb+PbO2+2H2SO4可知,放电时,Pb被氧化,应为电池负极反应,电极反应式为Pb-2e-+SO42-=PbSO4,正极上PbO2得电子被还原,电极反应式为PbO2+SO42-+2e-+4H+═PbSO4+2H2O,在充电时,阳极上发生氧化反应,阴极上发生还原反应,电极反应式和放电时的负极反应互为逆反应,以此解答.
| 充电 |
| 放电 |
解答:解;A.放电时,正极上PbO2得电子被还原,该电池的正极材料是PbO2,故A错误;
B.在充电时,阳极上发生氧化反应,和放电时的正极反应互为逆反应,即PbSO4-2e-+2H2O=PbO2+SO42-+4H+,故B正确;
C.充电时,反应总方程式为2PbSO4+2H2O=Pb+PbO2+2H2SO4,生成硫酸,硫酸浓度不变增大,故C错误;
D.放电时,正极上PbO2得电子被还原,电极反应式为PbO2+SO42-+2e-+4H+═PbSO4+2H2O,故D错误.
故选B.
B.在充电时,阳极上发生氧化反应,和放电时的正极反应互为逆反应,即PbSO4-2e-+2H2O=PbO2+SO42-+4H+,故B正确;
C.充电时,反应总方程式为2PbSO4+2H2O=Pb+PbO2+2H2SO4,生成硫酸,硫酸浓度不变增大,故C错误;
D.放电时,正极上PbO2得电子被还原,电极反应式为PbO2+SO42-+2e-+4H+═PbSO4+2H2O,故D错误.
故选B.
点评:本题考查了原电池和电解池原理,明确正负极、阴阳极上得失电子及电极反应是解本题关键,难点是电极反应式的书写,注意原电池正负极上发生的反应为电解池阳极、阴极上发生反应的逆反应,难度中等.

练习册系列答案
相关题目
电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,
电池总反应式为: 
则下列说法正确的是
| A.放电时:负极板上发生了还原反应 |
B.放电时:正极反应是 |
| C.充电时:铅蓄电池的负极应与充电器电源的正极相连 |
D.充电时:阳极反应是 |
 电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,如图所示.下列说法正确的是( )
电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,如图所示.下列说法正确的是( ) 电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为:Pb+PbO2+4H++2SO42-
电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为:Pb+PbO2+4H++2SO42- 2PbSO4+2H2O则下列说法正确的是( )
2PbSO4+2H2O则下列说法正确的是( )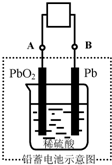 电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为:
电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为: