题目内容
现有一定量含
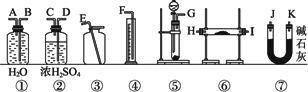
Na2O杂质的Na2O2试样,利用下图所示的实验装置可以测定其纯度.(可供选用的反应物只有CaCO3固体、6 mol/L盐酸、6 mol/L硫酸和蒸馏水)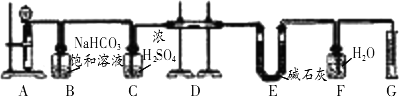
(1)实验前必须检查装置的气密性.仪器连接好后,在________中加适量的水,关闭装置A中分液漏斗的活塞后微热试管,若看到________,说明装置气密性好.
(2)装置A中的液体试剂应选用盐酸而不选用硫酸,理由是________.
(3)装置B的作用是________,装置C的作用是________,装置E中碱石灰的作用是________.
(4)装置D中发生反应的化学方程式为________.
(5)若开始时测得样品的质量为2.0 g,反应结束后测得气体的体积为224 mL(标准状况下),则Na2O2试样的纯度为________.
答案:
解析:
解析:
|
答案: (1)装置F(填G亦可) F中长导管内水面上升,停止加热一段时间后,水面下降(若填G,看到的现象是加热装置A后,G中导管口有气泡逸出)(2)硫酸与CaCO3固体反应生成的CaSO4微溶于水,会覆盖在CaCO3固体表面,使反应不能继续 (3)除去气体中的HCl 干燥气体 吸收装置D中剩余的CO2 (4)2Na2O2+2CO2 (5)78% 提示: (1)实验开始前首先要保证装置密闭,故要在F或G中加适量的水,关闭A中分液漏斗的活塞后微热试管,若看到F中长导管水面上升,停止加热一段时间后,水面下降,则说明装置的气密性好.(2)装置A中的液体试剂应选用盐酸,理由是硫酸与CaCO3固体反应生成的CaSO4微溶于水,会覆盖在CaCO3固体表面,阻碍硫酸与CaCO3固体反应. (3)装置B中饱和碳酸氢钠的作用是除去CO2气体中的HCl,装置C中浓硫酸的作用是干燥CO2气体,装置E中碱石灰的作用是吸收装置D中剩余的CO2. (4)装置D中发生的反应是CO2与Na2O和Na2O2的反应. (5)设Na2O2有x mol,Na2O有y mol,则78x+62y=2.0 g.由于反应结束后测得气体的体积为224 mL,此气体为O2,n(O2)=0.01 mol,而Na2O2~ |

练习册系列答案
相关题目