题目内容
升高温度,下列数据不一定增大的是( )
| A、弱电解质的电离常数 |
| B、反应的活化分子百分数 |
| C、化学平衡常数 |
| D、化学反应速率 |
考点:化学平衡的影响因素,化学反应速率的影响因素,弱电解质在水溶液中的电离平衡
专题:
分析:A、弱电解质的电离过程是吸热的,升高温度促进弱电解质的电离;
B、升高温度活化分子百分数增大,从而导致活化分子数目增大,有效碰撞次数增多;
C、根据勒夏特列原理,对所有可逆反应升温平衡都向吸热的方向移动.可逆反应的正反应既有吸热反应也有放热反应,要区别对待;
D、升高温度活化分子数目增大,有效碰撞次数增多,反应速率一定加快;
B、升高温度活化分子百分数增大,从而导致活化分子数目增大,有效碰撞次数增多;
C、根据勒夏特列原理,对所有可逆反应升温平衡都向吸热的方向移动.可逆反应的正反应既有吸热反应也有放热反应,要区别对待;
D、升高温度活化分子数目增大,有效碰撞次数增多,反应速率一定加快;
解答:
解:A、弱电解质的电离过程是吸热的,升高温度促进弱电解质的电离,升高温度电离程度增大,弱电解质的离子积一定增大,故A错误;
B、升高温度活化分子百分数增大,从而导致活化分子数目增大,有效碰撞次数增多,故B错误;
C、若正反应为放热反应,升高温度平衡向逆反应移动,化学平衡常数减小,若正反应为吸热反应,升高温度平衡向正反应移动,化学平衡常数增大,故C正确;
D、升高温度活化分子数目增大,有效碰撞次数增多,反应速率一定加快,故D错误;
故选:C.
B、升高温度活化分子百分数增大,从而导致活化分子数目增大,有效碰撞次数增多,故B错误;
C、若正反应为放热反应,升高温度平衡向逆反应移动,化学平衡常数减小,若正反应为吸热反应,升高温度平衡向正反应移动,化学平衡常数增大,故C正确;
D、升高温度活化分子数目增大,有效碰撞次数增多,反应速率一定加快,故D错误;
故选:C.
点评:本题考查温度对弱电解质的离子积、反应速率以及化学平衡常数的影响,比较基础.注意温度对化学反应速率和化学平衡影响的区别,不要混淆.

练习册系列答案
相关题目
萘环上碳原子的编号如(Ⅰ)式,根据系统命名法,(Ⅱ)式可称为2-硝基萘,则化合物(Ⅲ)的名称为( ) 

| A、2,5-二甲基萘 |
| B、1,4-二甲基萘 |
| C、4,7-二甲基萘 |
| D、1,6-二甲基萘 |
下列叙述正确的是( )
| A、将纯水加热,水的离子积变大、pH变小、溶液呈酸性 |
| B、pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)相等 |
| C、CH3COONa溶液加水稀释后,恢复至原温度,pH和Kw均减小 |
| D、中和等体积和等pH的盐酸和醋酸溶液所消耗的NaOH物质的量相同 |
有关水的电解实验,下列说法正确的是( )
| A、正、负极产生的气体质量比是1:2 |
| B、证明了水是由氢气和氧气组成 |
| C、与电源正极相连的一端产生氢气 |
| D、水能电解说明了分子是可分的 |
下列物质属于电解质的是( )
| A、铜 | B、稀硫酸 |
| C、二氧化碳 | D、熔融氯化钠 |
下列说法正确的是( )
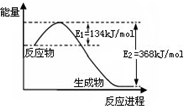

| A、已知1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化如图,则NO2和CO反应的热化学方程式为:NO2(g)+CO(g)=CO2(g)+NO(g);△H=+234 kJ?mol-1 |
| B、氯化铵溶液中加入足量的过氧化钠,仅产生一种气体 |
| C、25℃时,0.10 mol?L-1 NaHCO3溶液,加水稀释后,c(H+)与c(OH-)的乘积变小 |
| D、常温下,反应2A(s)+B(g)=2C(g)+D(g)不能自发进行,则该反应△H一定大于0 |
下列物质转化关系中,需要加入氧化剂才能实现的是( )
| A、Na2O2→O2 |
| B、MnO4-→Mn2+ |
| C、Fe2+→Fe3+ |
| D、CO2→HCO3- |
能正确表示下列反应的离子方程式是( )
| A、醋酸钠的水解反应:CH3COO-+H3O+=CH3COOH+H2O |
| B、碳酸氢钙与过量的NaOH溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
| C、向FeBr2溶液中通入过量氯气:2Fe2++Cl2═2Fe3++2Cl- |
| D、稀硝酸与过量的铁屑反应:3Fe+8H++2NO3-=3Fe3++2NO↑+4H2O |
如图X、Y、A、B、C均为短周期主族元素,下列说法不正确的是( )
| X | A | |
| Y | C | B |
| A、原子半径大小:Y>C>X>A |
| B、A、B的氢化物的稳定性:A>B |
| C、Y、C的最高价氧化物对应水化物的酸性:Y<C |
| D、B、C简单阴离子的还原性强弱为:B>C |