��Ŀ����
����Ŀ����ƻ�����㽶��ˮ���Ĺ����д�����������������ij��ѧ������ȤС�����������������Ϊԭ�Ϻϳ�������������ʵ�鲽�����£�
��һ���������������Ʊ�
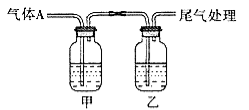
����50mL Բ����ƿ�У�����0.15mol�������� 0.12mol �����ᣬ�ټ���3��4��Ũ���ᣬҡ�ȣ�Ͷ��1��2����ʯ������ͼ��ʾ��װ����ˮ���Ļ�����Ӧװ�ã� ���ڷ�ˮ����Ԥ�ȼ���ˮ��ʹˮ���Ե��ڷ�ˮ����֧�ܿڡ�
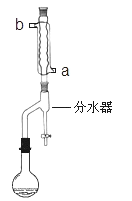
�ڴ�����ˮ��Բ����ƿ��ʯ��������С����ȡ��ڷ�Ӧ�����У�ͨ����ˮ���²����������Ϸֳ����ɵ�ˮ��ע�Ᵽ�ַ�ˮ����ˮ��Һ��ԭ���ĸ߶ȣ�ʹ�Ͳ㾡���ص�Բ����ƿ�С���Ӧ�ﵽ�յ��ֹͣ���ȣ���¼�ֳ���ˮ�������
��������Ʒ�ľ���
�۽���ˮ���ֳ�������ͷ�ӦҺһ�����Һ©���У��� 10 mL ��ˮϴ�ӡ��л��������10 mL10% Na2CO3 ϴ�������ԣ����� 10 mL ��ˮϴ�ӣ�����л���ת������ƿ�У�������ˮ����þ���
�ܽ���������������������50 mL ��ƿ�У���ѹ�����ռ� 124��126 �����֣���11.6g��Ʒ��
��1����ˮӦ�ô�������_____���� a �� b���ܿ�ͨ�롣
��2��������в��ϴӷ�ˮ���²��ֳ����ɵ�ˮ��Ŀ����_____��
��3�����й��ڷ�Һ©����ʹ��������ȷ����_____��
a����Һ©��ʹ��ǰ����Ҫ��©��ֻҪ��Һ©��������о����©ˮ����ʹ��
b����Һʱ����������Ӧ���Ͽڵ���
c����ȡ����Ӧ��ͼ��ʾ![]()
d���ų�Һ��ʱ���轫��������ʹ���ϵİ��۶�©�����ϵ�С��
��4����ʵ������У�������������������Է������� 116���IJ�����_____��
���𰸡�a ʹ�÷�ˮ�������ˮ��ʹƽ�������ƶ�����߷�Ӧ���� bd 83.3%
��������
�÷�Ӧ�����������������Ʊ�����������������Բ����ƿʹ���߷�Ӧ�������������������Լ��������������ӷ������Լ�װ����������ʹ��Ӧ���������������������߷�Ӧ���������ͬʱ������Բ����ƿ���ռ������֮����в�Ʒ�ľ��ƣ�������Ҫ������δ��Ӧ�������������ᣬ��һ�μ�ˮϴȥ���������ټ�̼���ƿ���ϴȥ��������������������ټ�ˮϴȥ̼���ƣ�֮���Һ����ˮ����þ����������������һ���������õ�������������������
(1)Ϊ����ǿ����Ч����ˮ��Ҫ����������ˮ��a��b����
(2)������ӦΪ���淴Ӧ�������������������ƽ�������ƶ�����߲��ʣ�
(3)a�������벣�������������Ƿ�©ˮ����a����
b���������������ܶȱ�ˮС��Ӧ���ϲ㣬���Դ��Ͽڵ�������b��ȷ��
c�� Ӧʹ��Һ©���ڳ��£�ʹ��Һ©���������ϣ����ڷ������ͷ�Һ©������ѹ����c����
d���ų�Һ��ʱ���轫��������ʹ���ϵİ��۶�©�����ϵ�С�ף�ƽ���Һ©������ѹ������Һ������d��ȷ��
��������ѡbd��
(4)�Ʊ������������ķ�Ӧ����ʽΪ��CH3COOH+CH3CH2CH2CH2OH![]() CH3COOCH2CH2CH2CH3+H2O�����ݷ�Ӧ����ʽ��֪��0.15mol�������� 0.12mol �����ᷴӦ����Ӧ����0.12mol CH3COOCH2CH2CH2CH3��������������Ϊ0.12mol��116g/mol=13.92g�����Բ���Ϊ
CH3COOCH2CH2CH2CH3+H2O�����ݷ�Ӧ����ʽ��֪��0.15mol�������� 0.12mol �����ᷴӦ����Ӧ����0.12mol CH3COOCH2CH2CH2CH3��������������Ϊ0.12mol��116g/mol=13.92g�����Բ���Ϊ![]() =83.3%��
=83.3%��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�