题目内容
【题目】下列实验结论正确的是( )
A.向某溶液中加入酚酞,溶液不变色,则该溶液一定显酸性
B.向某溶液中加入氯化钡溶液产生白色沉淀,再加入盐酸沉淀不消失,则该溶液中一定有 ![]()
C.向某溶液中加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,石灰水变浑浊,则原溶液中一定有 ![]()
D.向某溶液中滴加KSCN试剂,溶液变成血红色,则该溶液中一定有Fe3+
【答案】D
【解析】
A项、酚酞试液在中性溶液和酸性溶液中不变色,故A错误;
B项、某溶液中加入氯化钡溶液,有白色沉淀生成,再加盐酸酸化,沉淀不溶解,该溶液中可能含有SO42-或Ag+,但二者不能同时存在,故B错误;
C项、向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色无味气体,气体为二氧化硫或二氧化碳,则溶液中可能存在HCO3-、CO32-,故C错误;
D项、铁离子遇KSCN溶液为血红色,则某溶液中滴加KSCN溶液,变为血红色,则原溶液中含有Fe3+,故D正确;
故选D。

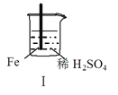
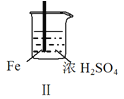
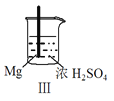
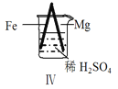
【题目】 Fe和Mg与H2SO4反应的实验如下:
实验 |
|
|
|
|
现象 | Fe表面产生大量无色气泡 | Fe表面产生气泡后迅速停止 | Mg表面迅速产生大量气泡 | Fe表面有大量气泡,Mg表面有少量气泡 |
关于上述实验说法不合理的是( )
A.I中产生气体的原因是:Fe + 2H+=Fe2++ H2↑
B.取出Ⅱ中的铁棒放入CuSO4溶液立即析出亮红色固体
C.Ⅲ中现象说明Mg在浓H2SO4中没被钝化
D.Ⅳ中现象说明Mg的金属性比Fe强
【题目】工业上,可采用还原法处理尾气中NO,其原理:2NO(g)+2H2(g)![]() N2(g)+2H2O(g) △H<0。在化学上,正反应速率方程式表示为v(正)=k(正)·cm(NO)·cn(H2),逆反应速率方程式表示为v(逆)=k(逆)·cx(N2)·cy(H2O),其中,k表示反应速率常数,只与温度有关,m,n,x,y叫反应级数,由实验测定。在恒容密闭容器中充入NO、H2,在T℃下进行实验,测得有关数据如下:
N2(g)+2H2O(g) △H<0。在化学上,正反应速率方程式表示为v(正)=k(正)·cm(NO)·cn(H2),逆反应速率方程式表示为v(逆)=k(逆)·cx(N2)·cy(H2O),其中,k表示反应速率常数,只与温度有关,m,n,x,y叫反应级数,由实验测定。在恒容密闭容器中充入NO、H2,在T℃下进行实验,测得有关数据如下:
实验 | c(NO)/mol·L-1 | c(H2)/mol·L-1 | v(正)/mol·L-1·min-1 |
① | 0.10 | 0.10 | 0.414k |
② | 0.10 | 0.40 | 1.656k |
③ | 0.20 | 0.10 | 1.656k |
下列有关推断正确的是
A. 上述反应中,反应物的总能量低于生成物的总能量
B. 若升高温度,则k(正)增大,k(逆)减小
C. 在上述反应中,反应级数:m=2,n=1
D. 在一定温度下,NO、H2的浓度对正反应速率影响程度相同