题目内容
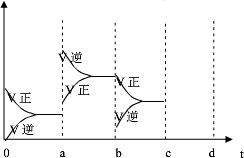
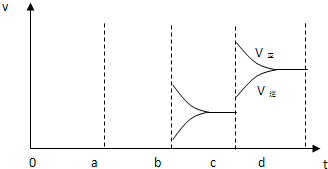
(1)如图表示在密闭容器中反应:2A(g)+3B(g)?C(g)+4D(s);△H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a到b过程中改变的条件可能是: ;b到c过程中改变的条件可能是 ;若增大压强时,反应速度变化情况画在c-d处 .
(2)反应2A?B+C,在某一温度时,达到平衡
①若温度升高,化学平衡常数变小,则正反应是 热反应.
②若B是固体,降低压强时,平衡向左移动,则A是 态.
③若A是气态,加压时,平衡不移动,则B为 态,C为 态.
【答案】分析:(1)根据正逆反应速率的变化结合温度、压强对反应速率和化学平衡的影响判断;
(2)①温度升高,化学平衡常数变小,说明平衡向逆反应方向移动,结合温度对平衡移动的影响分析;
②③可结合气体的化学计量数关系和压强对平衡移动的影响分析.
解答:解:(1)a时逆反应速率大于正反应速率,且正逆反应速率都增大,说明平衡应向逆反应方向移动,该反应的正反应放热,应为升高温度的结果,c时正反应速率不变,逆反应速率减小,在此基础上逐渐减小,应为减小生成物的原因,D为固体,应为减小C的浓度,若增大压强时,平衡向正反应方向移动,则正逆反应速率都增大,且正反应速率大于逆反应速率,图象应为 ,
,
故答案为:升高温度;减少C的浓度; ;
;
(2)①温度升高,化学平衡常数变小,说明平衡向逆反应方向移动,则正反应应为放热反应,故答案为:放热;
②若B是固体,降低压强时,平衡向左移动,即向气体体积增大的方向移动,则A为气体,故答案为:气;
③若A是气态,加压时,平衡不移动,说明反应前后气体的体积相等,则B、C应为气体,故答案为:气; 气.
点评:本题考查化学平衡移动的影响因素,题目难度不大,本题注意把握化学方程式的特征,结合外界条件对平衡移动的影响分析图象的曲线变化趋势.
(2)①温度升高,化学平衡常数变小,说明平衡向逆反应方向移动,结合温度对平衡移动的影响分析;
②③可结合气体的化学计量数关系和压强对平衡移动的影响分析.
解答:解:(1)a时逆反应速率大于正反应速率,且正逆反应速率都增大,说明平衡应向逆反应方向移动,该反应的正反应放热,应为升高温度的结果,c时正反应速率不变,逆反应速率减小,在此基础上逐渐减小,应为减小生成物的原因,D为固体,应为减小C的浓度,若增大压强时,平衡向正反应方向移动,则正逆反应速率都增大,且正反应速率大于逆反应速率,图象应为
 ,
,故答案为:升高温度;减少C的浓度;
 ;
;(2)①温度升高,化学平衡常数变小,说明平衡向逆反应方向移动,则正反应应为放热反应,故答案为:放热;
②若B是固体,降低压强时,平衡向左移动,即向气体体积增大的方向移动,则A为气体,故答案为:气;
③若A是气态,加压时,平衡不移动,说明反应前后气体的体积相等,则B、C应为气体,故答案为:气; 气.
点评:本题考查化学平衡移动的影响因素,题目难度不大,本题注意把握化学方程式的特征,结合外界条件对平衡移动的影响分析图象的曲线变化趋势.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目

 (1)对于下列反应:2SO2+O2?2SO3,如果2min内SO2的浓度由6mol/L下降为2mol/L,那么,用SO2浓度变化来表示的化学反应速率为
(1)对于下列反应:2SO2+O2?2SO3,如果2min内SO2的浓度由6mol/L下降为2mol/L,那么,用SO2浓度变化来表示的化学反应速率为 汽车内燃机工作时产生的高温会引起N2和O2发生反应生成NO气体,是导致汽车尾气中含有NO的原因之一.
汽车内燃机工作时产生的高温会引起N2和O2发生反应生成NO气体,是导致汽车尾气中含有NO的原因之一.