题目内容
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、常温、常压下,16 g O3中含有的氧原子数为NA |
| B、7.8 g Na2O2与水充分反应,转移的电子数为0.2 NA |
| C、0.1 mol Fe与0.1 mol Cl2充分反应,转移的电子数为0.3NA |
| D、标准状况下,11.2 L H2O中含有的氢原子数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.1个O3含有的氧原子数为3个,质量和微粒数目之间的关系式:N=nNA;
B.根据过氧化钠的物质的量和O元素的化合价分析;
C.等物质的量铁和氯气反应生成氯化铁,铁过量,反应的电子转移根据氯气计算;
D.标准状况下,水的状态不是气体.
B.根据过氧化钠的物质的量和O元素的化合价分析;
C.等物质的量铁和氯气反应生成氯化铁,铁过量,反应的电子转移根据氯气计算;
D.标准状况下,水的状态不是气体.
解答:
解:A.O3是氧的单质,只含有氧原子,1个O3含有的氧原子数为3个,所以16gO3中所含氧原子个数为:N=nNA×3=
×3×NA=NA,故A正确;
B.7.8g过氧化钠为0.1mol,与足量水反应,自身发生氧化还原反应,转移电子数为0.1NA,故B错误;
C.等物质的量铁和氯气反应生成氯化铁,铁过量,反应的电子转移根据氯气计算,转移电子数0.2NA,故C错误;
D.标况下水不是气体,不能使用标况下的气体摩尔体积计算22.4L水的物质的量,故D错误;
故选:A.
| 16g |
| 48g/mol |
B.7.8g过氧化钠为0.1mol,与足量水反应,自身发生氧化还原反应,转移电子数为0.1NA,故B错误;
C.等物质的量铁和氯气反应生成氯化铁,铁过量,反应的电子转移根据氯气计算,转移电子数0.2NA,故C错误;
D.标况下水不是气体,不能使用标况下的气体摩尔体积计算22.4L水的物质的量,故D错误;
故选:A.
点评:本题考查阿伏加德罗常数的有关计算和判断,明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,题目难度不大.

练习册系列答案
相关题目
化学知识在生产和生活中有着重要的应用.下列说法中正确的是( )
①铝制餐具不宜用蒸煮或长时间存放酸性、碱性或咸的食物
②发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔
③纯净的二氧化硅是现代光学及光纤制品的基本原料
④Na2O2既可作呼吸面具中O2的,又可漂白织物、麦杆、羽毛等
⑤碳酸钠在医疗上是治疗胃酸过多的一种药剂
⑥明矾常作为消毒剂.
①铝制餐具不宜用蒸煮或长时间存放酸性、碱性或咸的食物
②发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔
③纯净的二氧化硅是现代光学及光纤制品的基本原料
④Na2O2既可作呼吸面具中O2的,又可漂白织物、麦杆、羽毛等
⑤碳酸钠在医疗上是治疗胃酸过多的一种药剂
⑥明矾常作为消毒剂.
| A、①②③④ | B、①②③⑤ |
| C、①②④⑥ | D、①②③④⑤⑥ |
下列说法正确的是( )
| A、溶液、胶体和浊液的本质区别在于分散质粒子的直径不同 |
| B、金属氧化物都属于碱性氧化物 |
| C、非金属氧化物都属于酸性氧化物 |
| D、氧化还原反应的本质是化合价发生升降 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、等物质的量的N2和CO所含有的原子数均为2NA |
| B、通常状况下,64g SO2中含有的分子数为NA |
| C、标准状况下,22.4L CH4和O2的混合气体所含有的分子数为2NA |
| D、物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、6.72L NO2与水充分反应转移的电子数目为0.2NA |
| B、12.0g NaHSO4固体中含有的阳离子数为0.2NA |
| C、用含0.01 mol KI的稀溶液制取碘化银胶体时,产生胶体粒子0.01NA个 |
| D、常温下体积相同容器分别装有质量相同的N2、CO气体,产生的压强相同 |
下列说法中正确的是( )
| A、1 L 水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L |
| B、从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液的浓度为1 mol/L |
| C、配制500 mL 0.2 mol/L的CuSO4溶液,需称量CuSO4固体的质量为16.0g |
| D、中和100 mL 1 mol/L的H2SO4溶液,需NaOH的质量为4.0g |
下列说法不正确的是( )
| A、溶液、胶体和悬浊液这三种分散系的本质区别是能否透过滤纸或半透膜 |
| B、仅用新制的氢氧化铜悬浊液一种试剂可鉴别乙醇、甘油、乙醛、乙酸、乙酸乙酯、葡萄糖溶液(必要时可加热) |
C、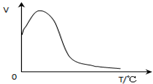 过氧化氢在酶催化作用下的分解反应速率随温度的变化关系如图所示 |
| D、工业上从海带中提取碘单质,经历的步骤有浸泡-过滤-氧化-结晶-粗碘提纯 |