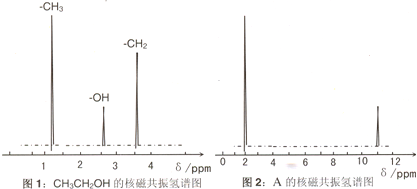
题目内容
 以乙烯为原料,可以制备乙酸乙酯
以乙烯为原料,可以制备乙酸乙酯
(1)③的反应类型是
酯化反应
酯化反应
.(2)乙醇分子中官能团的名称是
羟基
羟基
,乙醇与水均能和金属钠反应,反应现象说明乙醇羟基中的氢原子不如水分子中的氢原子活泼
乙醇羟基中的氢原子不如水分子中的氢原子活泼
(用简要文字说明).写出
 与足量金属钠反应的化学方程式
与足量金属钠反应的化学方程式

(3)利用图示装置制取乙酸乙酯.写出生成乙酸乙酯的化学方程式:
CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O
| 浓H2SO4 |
| △ |
CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O
;| 浓H2SO4 |
| △ |
(4)实验操作中,
为了加快反应速率,采取的措施是
加热
加热
、加入浓硫酸
加入浓硫酸
,出于对实验安全的考虑,采取的措施是
浓硫酸在乙醇之后加入
浓硫酸在乙醇之后加入
、在左边的试管中加入沸石、导管口不能插入饱和碳酸钠溶液中;
在左边的试管中加入沸石、导管口不能插入饱和碳酸钠溶液中;
(上述措施各举两个例子即可);(5)乙酸乙酯也可由下述反应制得
冰醋酸+
CH2=CH2
CH2=CH2
| 磷酸盐 |
分析:(1)用乙烯为原料制备乙酸乙酯时,先用乙烯和水发生加成反应制备乙醇,然后用乙醇氧化后生成乙酸,乙醇乙酸发生酯化反应制得乙酸乙酯;
(2)醇的官能团为羟基,羟基氢原子的活泼性不同,反应进行的剧烈程度不同,水是弱电解质,乙醇是非电解质;
(3)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应;
(4)酯化反应是可逆的,从化学平衡角度分析,乙酸与乙醇反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动;加入药品时,为防止酸液飞溅,应先加入乙醇再加入浓硫酸和乙酸;液体加热要加碎瓷片,防止暴沸;饱和碳酸钠溶液与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层;导管伸入液面下可能发生倒吸;(5)根据质量守恒进行解答.
(2)醇的官能团为羟基,羟基氢原子的活泼性不同,反应进行的剧烈程度不同,水是弱电解质,乙醇是非电解质;
(3)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应;
(4)酯化反应是可逆的,从化学平衡角度分析,乙酸与乙醇反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动;加入药品时,为防止酸液飞溅,应先加入乙醇再加入浓硫酸和乙酸;液体加热要加碎瓷片,防止暴沸;饱和碳酸钠溶液与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层;导管伸入液面下可能发生倒吸;(5)根据质量守恒进行解答.
解答:解:(1)用乙烯为原料制备乙酸乙酯时,先用乙烯和水发生加成反应制备乙醇,然后用乙醇氧化后生成乙酸,乙醇乙酸发生酯化反应制得乙酸乙酯,发生的反应分别为:
CH2=CH2+H2O
CH3CH2OH,2CH3CH2OH+O2
2CH3CHO+H2O,2CH3CHO++O2
2CH3COOH,CH3CH2OH+CH3COOH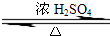 CH3COOCH2CH3+H2O,该反应为本质为酸脱羟基,醇脱氢,是酯化反应,
CH3COOCH2CH3+H2O,该反应为本质为酸脱羟基,醇脱氢,是酯化反应,
故答案为:酯化反应;
(2)乙醇分子式为CH3CH2OH,是乙基和羟基连接形成的,官能团名称为羟基;羟基氢原子的活泼性不同,反应进行的剧烈程度不同,水是弱电解质,乙醇是非电解质;乙醇分子中的羟基氢原子不如水分子中的氢原子活泼,与钠反应的剧烈程度小;醇中的羟基和钠反应生成氢气, ,
,
故答案为:羟基;乙醇羟基中的氢原子不如水分子中的氢原子活泼; ;
;
(3)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,同时该反应可逆,反应的化学方程式为CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O,
故答案为:CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O;
(4)化学反应温度高,反应快,酯化反应是可逆过程,乙酸与乙醇反应,浓硫酸吸水有利于平衡向生成乙酸乙酯方向移动,提高原料利用率;浓硫酸溶于水放出大量的热,加入药品时,为防止酸液飞溅,应先加入乙醇再加入浓硫酸和乙酸,液体乙酸乙醇沸点低,加热要加碎瓷片,防止暴沸;导管不能插入溶液中,导管要插在饱和碳酸钠溶液的液面上,伸入液面下可能发生倒吸,
故答案为:加热、加入浓硫酸;浓硫酸在乙醇之后加入;在左边的试管中加入沸石;导管口不能插入饱和碳酸钠溶液中;
(5)乙酸乙酯的化学式为C4H8O2,冰醋酸的化学式为,C2H4O2,根据质量守恒定律知未知物为C2H4,结合已知条件,冰醋酸+
乙酸乙酯,由此可得为未知物为乙烯,
故答案为:CH2=CH2.
CH2=CH2+H2O
| 催化剂 |
| 催化剂 |
| 催化剂 |
| 加热 |
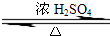 CH3COOCH2CH3+H2O,该反应为本质为酸脱羟基,醇脱氢,是酯化反应,
CH3COOCH2CH3+H2O,该反应为本质为酸脱羟基,醇脱氢,是酯化反应,故答案为:酯化反应;
(2)乙醇分子式为CH3CH2OH,是乙基和羟基连接形成的,官能团名称为羟基;羟基氢原子的活泼性不同,反应进行的剧烈程度不同,水是弱电解质,乙醇是非电解质;乙醇分子中的羟基氢原子不如水分子中的氢原子活泼,与钠反应的剧烈程度小;醇中的羟基和钠反应生成氢气,
 ,
,故答案为:羟基;乙醇羟基中的氢原子不如水分子中的氢原子活泼;
 ;
;(3)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,同时该反应可逆,反应的化学方程式为CH3COOH+CH3CH2OH
| 浓H2SO4 |
| △ |
故答案为:CH3COOH+CH3CH2OH
| 浓H2SO4 |
| △ |
(4)化学反应温度高,反应快,酯化反应是可逆过程,乙酸与乙醇反应,浓硫酸吸水有利于平衡向生成乙酸乙酯方向移动,提高原料利用率;浓硫酸溶于水放出大量的热,加入药品时,为防止酸液飞溅,应先加入乙醇再加入浓硫酸和乙酸,液体乙酸乙醇沸点低,加热要加碎瓷片,防止暴沸;导管不能插入溶液中,导管要插在饱和碳酸钠溶液的液面上,伸入液面下可能发生倒吸,
故答案为:加热、加入浓硫酸;浓硫酸在乙醇之后加入;在左边的试管中加入沸石;导管口不能插入饱和碳酸钠溶液中;
(5)乙酸乙酯的化学式为C4H8O2,冰醋酸的化学式为,C2H4O2,根据质量守恒定律知未知物为C2H4,结合已知条件,冰醋酸+
| 磷酸盐 |
故答案为:CH2=CH2.
点评:本题考查了乙酸乙酯的制备,解答时须注意酯化反应的原理和用乙烯为原料制备乙酸乙酯的反应原理,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目