��Ŀ����
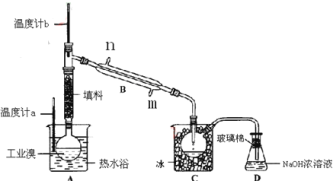
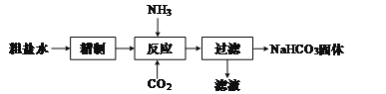
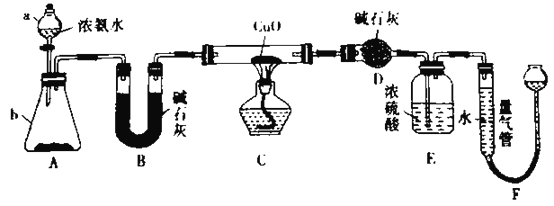
����Ŀ��ijС��������CuO��NH3��Ӧ���о�NH3��ij�����ʲ��ⶨ����ɣ����������ʵ��װ��(�г�װ��δ����)����ʵ�飺
�ش��������⣺
(l)����a������Ϊ____________������b�п�ѡ����Լ�Ϊ___________��
(2)ʵ�����У�����װ��A��������ȡ����ɫ������___________(����)��
A.Cl2 B.O2 C.NO2 D.CO2
(3)ʵ���й۲쵽װ��C�к�ɫCuO��ĩ��Ϊ��ɫ���壬����������ɫ��ζ�������������������֤��MH3����_______�ԣ�װ��C�з�����Ӧ�Ļ�ѧ����ʽΪ___��
(4)װ��E��Ũ�����������___________��
(5)��ȡ�������ǰ��Ӧ��װ��F���еIJ�����________��
(6)ʵ����ϣ������װ��D����m g��װ��F�ⶨ��������Ϊn L(�Ѳ���ɱ�״��)�������е������ԭ�Ӹ�����Ϊ_______________(�ú�m��n��ĸ�Ĵ���ʽ��ʾ)��
���𰸡���Һ©�� �����ƻ��������ƹ�����ʯ�� BD ��ԭ 2NH3+3CuO![]() 3Cu+N2+3H2O ����δ��Ӧ�İ�������ֹF��ˮ��������D ���������ƶ��ұ�©����ʹ��������Һ����ƽ
3Cu+N2+3H2O ����δ��Ӧ�İ�������ֹF��ˮ��������D ���������ƶ��ұ�©����ʹ��������Һ����ƽ ![]()
��������
(1)���������Ĺ����֪������a�Ƿ�Һ©����Ũ��ˮ��������ʯ�ҡ��������ƹ��塢��ʯ�ҵ���ȡ������������b�п�ѡ����Լ�Ϊ�����ƻ��������ƹ�����ʯ�ң�
(2)װ��A��һ�ֹ���+Һ�巴Ӧ����Ҫ���ȵ����巢��װ�ã�����������ȡH2��CO2��NO2�ȣ���������H2O2��MnO2����ȡO2������ע������ɫ���壬������NO2����ѡBD��
(3)��ɫCuO��ĩ��Ϊ��ɫ���壬˵����ɫ��CuO����ԭΪCu��ͬʱNH3������ΪN2��֤����NH3���л�ԭ��:2NH3+3CuO![]() 3Cu+N2+3H2O��
3Cu+N2+3H2O��
(4)ʵ����Ҫͨ������Dװ�÷�Ӧǰ�������������Ϊ��������ԭ�����ʵ����ļ������ݣ�����Eװ�þ��и���D��F�����ã���ֹF�е�ˮ��������D�У�ͬʱ����δ��Ӧ��NH3���յ����ʴ�Ϊ����δ��Ӧ�İ�������ֹF��ˮ��������D��
(5)�ⶨ�������ռ��������ʱҪ��֤װ��������ѹǿ�����ѹ��ȣ�������Ҫ�����������ƶ��ұ�©����ʹ��������Һ����ƽ��
(6)D������������NH3��ԭCuO���ɵ�ˮ��������
n(H)=![]() ��2=
��2=![]() mol��
mol��
n(N)=![]() ��2=
��2= ![]() mol��
mol��
���������е������ԭ�Ӹ�����Ϊ:![]() mol��
mol��![]() mol =
mol =![]() ��
��

����Ŀ����ͼ��ʾ������������̽��NH3�����ʡ�ʵ��ʱ��NaOH�����ϵμ���Ũ��ˮ����������һ������������档�±��ж�ʵ�����������Ľ�����ȷ����(����)

ѡ�� | ʵ������ | ���� |
A | Ũ���ḽ���������� | NH3��Ũ���ᷴӦ������NH4Cl���� |
B | Ũ���ḽ������������ | NH3��Ũ���������Ӧ |
C | �Ȼ�����Һ����� | ����Һһ����AlCl3��Һ |
D | �����ʯ����ֽ����ɫ��ʪ���ʯ����ֽ���� | NH3��һ�ֿ����Լ� |
A.AB.BC.CD.D