题目内容
可以将不同元素的原子形成阴离子或阳离子的倾向用相应的数值x表示。若x值越大,则该元素的原子越容易得到电子,不易失去电子,即形成阴离子的倾向大,非金属性较强。反之,则表示形成阳离子的倾向大,元素的金属性相对较强。下表中提供的是部分短周期元素的x的值:
元素 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
x | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
请回答下列问题:
(1)结合元素周期表的结构(周期、主族),推测元素的x值与原子半径的变化关系是____________。
指出元素周期表中,x值最小的元素位于____________(放射性元素除外)。
(2)分析N和Mg的x值范围为:
____________<x(N)<____________;
____________<x(Mg)<____________。
(3)若两元素的x值的差(Δx)大于1.7时,成键时一般形成离子键;小于1.7时,一般为共价键。则PCl3的电子式为____________;化合物BeCl2、LiCl熔点:BeCl2____________LiCl(填“>”“<”或“=”)。
(1)同周期(同主族)元素随着原子半径减小,其x值增加 第6周期、ⅠA族
(2)2.55 3.44 0.93 1.57
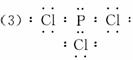 <
<
解析:由x值及周期律知识可得出结论:同周期元素(如Li→F,Na→Cl),原子半径逐渐减小,而x值逐渐增大,同主族元素,随原子序数增加,x值减小。故x值最小的应是第6周期的ⅠA族元素,即Cs。由以上规律可推导出N、Mg的x值应分别在C、O及Na、Al之间。由Be、Cl的x值,可知3.16-1.57=1.59<1.7,故BeCl2为共价化合物,而LiCl则为离子化合物,其熔点为LiCl>BeCl2。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
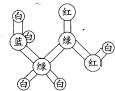 2008年诺贝尔化学奖获得者钱永健对我们理解绿色荧光蛋白如何发光作出了贡献,他还将颜色标签扩展至除绿色之外的颜色,以便可以用各种颜色标识不同的细胞.下图是一个分子的球棍模型图,它是蛋白质水解的产物之一,图中“棍”代表单键、双键或叁键.不同颜色的球代表不同元素的原子,其原子序数为1~10.该模型图表示的分子具有的性质是( )
2008年诺贝尔化学奖获得者钱永健对我们理解绿色荧光蛋白如何发光作出了贡献,他还将颜色标签扩展至除绿色之外的颜色,以便可以用各种颜色标识不同的细胞.下图是一个分子的球棍模型图,它是蛋白质水解的产物之一,图中“棍”代表单键、双键或叁键.不同颜色的球代表不同元素的原子,其原子序数为1~10.该模型图表示的分子具有的性质是( )| A、只能与盐酸反应,不能与氢氧化钠反应 | B、只能与氢氧化钠反应.不能与盐酸反应 | C、既能与盐酸反应,又能与氢氧化钠反应 | D、既不能与盐酸反应.又不能与氢氧化钠反应 |

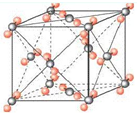
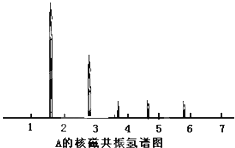 为测定某有机化合物A的结构,进行如下实验.
为测定某有机化合物A的结构,进行如下实验.