题目内容
【题目】下列有关化学反应速率和化学平衡影响的图象,其中图象和实验结论表达错误的是




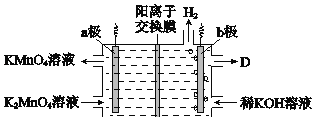
A. a是其他条件一定时,反应速率随温度变化的图象,正反应ΔH > 0
B. b是在有无催化剂存在下建立的平衡过程图象,Ⅰ是使用催化剂时的曲线
C. c是一定条件下,向含有一定量A的容器中逐渐加入B时的图象,压强p1 > p2
D. d是在平衡体系的溶液中溶入少量KCl固体后化学反应速率随时间变化的图象
【答案】CD
【解析】
A.升高温度,平衡向吸热方向移动,根据反应方向判断反应热; B.催化剂能同等程度的改变正逆反应速率,平衡不移动; C. A的转化率随着B的增加而增大;D.氯化钾不影响平衡移动。
A.根据图象知,升高温度,平衡向正反应方向移动,则正反应的△H>0,故A正确; B.使用催化剂,反应速率加快,缩短反应时间,所以先达到平衡状态,所以a是使用催化剂时的曲线,故B正确; C.不断加入B,A的转化率增大,故C错误; D.该反应实质为Fe3++3SCN-![]() Fe(SCN)3,钾离子和氯离子不参加反应,则KCl浓度增大化学平衡不移动,故D错误;选CD。
Fe(SCN)3,钾离子和氯离子不参加反应,则KCl浓度增大化学平衡不移动,故D错误;选CD。

 通城学典默写能手系列答案
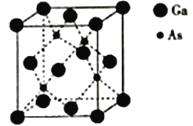
通城学典默写能手系列答案【题目】镍与VA族元素形成的化合物是重要的半导体材料,应用最广泛的是砷化镓(GaAs),回答下列问题:
(1)基态Ga原子的核外电子排布式为_____,基态As原子核外有_________个未成对电子。
(2)镓失去电子的逐级电离能(单位:kJ·mol-1)的数值依次为577、1984.5、2961.8、6192由此可推知镓的主要化合价为____和+3。砷的电负性比镍____(填“大”或“小”)。
(3)比较下列镓的卤化物的熔点和沸点,分析其变化规律及原因:________________________。
镓的卤化物 | GaCl3 | GaBr3 | GaI3 |
熔点/℃ | 77.75 | 122.3 | 211.5 |
沸点/℃ | 201.2 | 279 | 346 |
GaF3的熔点超过1000℃,可能的原因是___________________________________________。
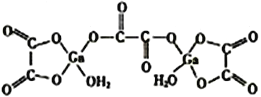
(4)二水合草酸镓的结构如图所示,其中镓原子的配位数为______,草酸根中碳原子的杂化方式为______________。
(5)砷化镓熔点为1238℃,立方晶胞结构如图所示,晶胞参数为a=565pm。该晶体的类型为_________,晶体的密度为___________(设NA为阿伏加德罗常数的数值,列出算式即可)g·cm-3。